Бугристость подвздошной кишки. Пальпация червеобразного отростка
Обновлено: 22.04.2024
Болезнь Крона представляет собой хроническое гранулематозное воспаление желудочно-кишечного тракта с преимущественным поражением терминального отдела подвздошной кишки. В результате хронического воспаления развивается рубцовая ткань, что приводит к стенозу просвета кишки.
Для болезни Крона характерно сегментарное поражение кишечника, имеющее четкую границу с соседними здоровыми отделами. Стенка кишки утолщена, просвет ее сужен на участке поражения, расширен перед стенозированным участком. Слизистая также утолщена, бугристая, с многочисленными щелевидными язвами и трещинами, имеет вид «булыжной мостовой». При микроскопии во всей толще кишки определяется воспалительный инфильтрат, а также характерные гранулемы из эпителиоидных клеток и гигантских многоядерных клеток.
Клиническая картина довольно разнообразна. В ней можно выделить местные и общие симптомы, а также внекишечные проявления заболевания. Общие симптомы: слабость, усталость, повышение температуры, часто волнообразного характера. Местные «кишечные» симптомы: боль в животе, часто симулирующая острый аппендицит, понос, анорексия, тошнота, рвота, вздутие кишечника, потеря веса. В патологический процесс вовлекаются многие органы и системы, он нередко осложняется прободением стенки кишки с развитием внутрибрюшных абсцессов, перитонита, внутренних и наружных свищей, стриктур, брюшных спаек; кишечной непроходимостью, кровотечением. Потеря веса наблюдается у значительного числа больных и обусловлена сначала анорексией и усилением боли после приема пищи, а в запущенных случаях и синдромом нарушения всасывания в кишечнике.
Диагностика болезни Крона является трудной задачей в ургентной хирургии, что обусловлено малой информативностью общедоступных методов инструментального исследования при данной патологии, таких как обзорная рентгенография брюшной полости, пассаж бария по желудочно-кишечному тракту, УЗИ органов брюшной полости. В то же время наиболее информативные современные методы диагностики данной патологии в виде компьютерной томографии брюшной полости, видеокапсульной эндоскопии кишечника и инструментально-ассистированной энтероскопии находят малое применение в условиях ургентной хирургии. В силу этих обстоятельств болезнь Крона чаще всего диагностируется как операционная находка.
Под нашим наблюдением находились 8 больных, подвергшихся операции в хирургическом отделении ГУЗ “РКБ №1” с 1988 по 2015 гг. Возраст больных от 20 до 60 лет. Из них трое больных женского, пятеро мужского пола. Все больные оперированы с дооперационными предположительными диагнозами: 1 больной с диагнозом: перформативная язва желудка; 3 больных с диагнозом: острый аппендицит; 4 больных с диагнозом: острая кишечная непроходимость. У больных наблюдались тошнота, рвота, учащение пульса, повышение температуры тела до 40*С, вздутие живота, диарея, лейкоцитоз со сдвигом влево. При пальпации определялось напряжение мышц передней брюшной стенки, слабо выраженные симптомы раздражения брюшины.
Хирургическая тактика заключалась у больного с подозрением на перформативную язву желудка в срединной лапаротомии, санации и дренирования брюшной полости после установления диагноза болезни Крона на уровне тощей кишки.
У 3 больных с дооперационным диагнозом: острый аппендицит была выявлена болезнь Крона на уровне подвздошной кишки, вторичные воспалительные изменения червеобразного отростка. Операция заканчивалась аппендэктомией, санацией и дренированием брюшной полости.
У 4 больных с выраженной клинической картиной острой кишечной непроходимости после выявления участков стеноза гранулематозно измененных участков кишки производились резекции кишечника с последующими тотальными интубациями через илеостомы, дренирования брюшной полости.
В послеоперационном периоде у больных применялись инфузионная терапия, препараты типа салазопиридазина, глюкокортикоиды, антибиотики.
Все больные выписаны с улучшением, с рекомендациями последующего наблюдения и лечения у гастроэнтеролога.
Для подтверждения сказанного сошлемся на следующее клиническое наблюдение.
Больной Т., 59 лет, находившийся на лечении в пульмонологическом отделении ГУЗ “РКБ №1” по поводу хронического бронхита, почувствовал боли в животе схваткообразного характера. Был осмотрен дежурным хирургом. Рекомендована очистительная клизма. После клизмы состояние несколько улучшилось, отошли газы, стула не было. Через 30-40 минут снова появились боли, тошнота, была однократная рвота. Заподозрена кишечная непроходимость. На рентгенограмме в правой половине брюшной полости определяются чаши Клойбера-Шварца, жидкость в них на разных уровнях. После двухчасового наблюдения улучшения состояния больного не наступило, вздутие живота, усиленная периодическая перистальтика, шум плеска продолжали сохраняться. С диагнозом “острая кишечная непроходимость” больной взят на операцию. Обнаружено наличие гиперемированных отечных петель подвздошной кишки с наличием множества гранул на серозных покровах. Отступя на 20 см от илеоцекального угла, на протяжении 15 см отмечено сужение просвета измененного участка кишки. Проксимальнее этого участка кишечные петли раздуты, а дистальные отделы спавшиеся. Произведена резекция измененного отдела подвздошной кишки на протяжении 70 см с наложением илеостомы и тотальной интубацией тонкого кишечника. Болезнь Крона гистологически подтверждена. В послеоперационном периоде назначена консервативная терапия: преднизолон, сульфасалазин, антибиотики, инфузионная терапия. Послеоперационный период протекал без осложнений. Больной выписан домой с рекомендацией проведения курсов противорецидивного лечения болезни Крона.
1.Трудности диагностики болезни Крона обусловлены многообразием форм проявления.
2. Дооперационная диагностика болезни Крона должна быть комплексной, с обязательным включением компьютерной томографии органов брюшной полости в стандарт диагностики.
3. Хирургическая тактика при болезни Крона диктуется операционной находкой.
Бугристость подвздошной кишки. Пальпация червеобразного отростка
Бугристость подвздошной кишки. Пальпация червеобразного отростка
Уже проф. Образцов обратил внимание на бугристость ilei при тяжелых случаях брюшного тифа, вследствие глубокой инфильтрации стенки кишки на месте Пейровых бляшек и придавал этой бугристости дурное прогностическое значение. В этих случаях брюшного тифа, по мнению Образцова, можно ожидать прободения или значительного кишечного кровотечения.
Но иногда и при туберкулезных язвах удается констатировать по бугристости стенки присутствие рубца в кишке, особенно, в тех случаях, когда рубцующаяся язва вызывает сужение и гипертрофию мускулатуры в кишке выше язвы. В этих обоих случаях ileum представляется не только бугристым, но нередко благодаря раздражению брюшины пальпация его делается болезненной.
Нечего говорить, что во всех случаях стеноза в области слепой кишки, часто у илеоцекального клапана, прощупывающийся ileum представляется значительно большего диаметра — иногда толщиной в 2 - 3 пальца, с плотными утолщенными стенками и всегда переполнен содержимым, дающим шум плеска; при этом он энергично перистальтирует.
Подобное изменение в свойствах ilei настолько характерно для сужения ниже его, что позволяет диагностировать сужение в самом его начале; поэтому знакомство с пальпаторными ощущениями от нормальной кишки крайне необходимо.

Но если ileum не переполнен содержимым и при том энергично перистальтирует, то при пальпации он представляется в форме тонкого, в карандаш толщиной, не урчащего плотного цилиндрика. Не совсем опытного пальпатора подобное состояние кишки может вовлечь в заблуждение и подать повод к ошибочному толкованию—принять подвздошную кишку за прощупывающийся appendix.
Это, повидимому, случилось с Iaworski'м, Lapinski'м, Орловским и др., утверждающими, что червеобразный отросток в нормальном состоянии прощупывается очень часто (49% Орловский, 51% Iaworski и Lapinski), a ileum редко. Следовательно, для того, чтобы избежать указанной ошибки, нужно, с одной стороны, овладеть техникой пальпации ilei, с другой, нужно уметь прощупывать нормальный или патологически измененный отросток слепой кишки и уметь проводить между ними пальпаторную дифференциальную диагностику.
Пальпацией отростка слепой кишки в последнее время занималось довольно много клиницистов; надо сказать, что результаты их исследований настолько противоречивы и подчас удивительны, что работы эти невольно подвергаются большому сомнению, а статистика большой критике.
В то время как Еdebоls утверждает, что он может прощупать всякий здоровый червеобразный отросток, Орловский пальпирует его в 49%, Iaworski и Lapinski в 51%, Рудницкий в 27%,— Гаусман прощупывает нормальный отросток не чаще чем в 16% всех случаев, при чем прибавляет, что „значительная часть этих отростков несомненно являются патологически измененными, в виду чего % прощупываемости нормального отростка гораздо меньше этой цифры."
Эта скромная статистика Гаусмана вполне согласуется с наблюдениями проф. Образцова и его клиники, где детально разрабатывалась пальпация органов брюшной полости и где даже более или менее ясно прощупывающийся отросток всегда принимался за таковой с определенной оговоркой: „вероятно отросток"; вот почему ни в одной работе как самого проф. Образцова, так и его учеников % прощупываемости здоровых отростков не выведен—ибо с уверенностью вывести его невозможно. Более смело к этому вопросу подошел Гаусман и разобрав обстоятельно технику пальпации и всю возможность смешения отростка с другими образованиями дал все-таки определенные выводы.
Этим я не хочу сказать, что прщупать здоровый отросток вовсе нельзя; я хочу только подчеркнуть, что никогда нельзя быть уверенным, что принимаемое при пальпации, похожее по форме на отросток, образование, действительно является червеобразным отростком слепой кишки, а не дупликатурой брыжейки, лимфатическим тяжем, краем брыжейки, спастически сокращенной петлей кишки, брюшком подвздошной мышцы и пр. Совершенно иначе обстоит дело в том случае, если отросток при воспалительном процессе изменен—в этом случае довольно часто его можно прощупать, и хотя ошибки и возможны, но у опытного исследователя они все-таки редки.
В чем же, спрашивается, кроются причины невозможности с уверенностью прощупать нормальный червеобразный отросток?
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Нейроэндокринная опухоль червеобразного отростка

Нейроэндокринные опухоли (НЭО) представляют собой редко встречающиеся новообразования, интерес к которым не ослабевает с 1902 г., когда они были выделены в отдельную группу немецким патологоанатомом Обендорфером [1].
Клинически НЭО червеобразного отростка может быть как функционирующей, так и не функционирующей – эти опухоли составляют 15-30% случаев 5. Функционирующие НЭО проявляются карциноидным синдромом.
Надо отметить, что цианоз или покраснение кожи лица и шеи часто является первым, а иногда единственным симптомом заболевания. Эту «маску» у женщин чаще всего принимают за климактерические приливы, особенно если учесть, что частота заболеваемости НЭО увеличивается после 50 лет. Также жалобы могут расцениваться как вегетативные реакции при неврозах или нейроциркуляторной дистонии, что отодвигает сроки распознавания заболевания 4.
Абдоминальные проявления (схваткообразные боли в животе, тошнота, рвота, диарея) напрямую обусловлены влиянием на моторику ЖКТ серотонина, однако конкурирующими причинами могут быть ишемия кишки, раздражение брыжейки, явления непроходимости, как и в случае с нефункционирующей НЭО. Физикальное обследование на поздних стадиях заболевания может выявить наличие пальпируемой опухоли в брюшной полости, изменения периферических регионарных лимфоузлов 5.
Необходимо особо остановиться на сердечно-сосудистой симптоматике карциноидного синдрома, которая характеризуется тахикардией, болями в области сердца, повышением артериального давления (АД). Эти жалобы очень часто встречаются в повседневной практике терапевта и кардиолога, и на рутинном приеме достаточно трудно заподозрить у пациента карциноидную опухоль, а не более частую и известную клиницистам сердечно-сосудистую патологию.
Высокие концентрации циркулирующих биологически активных аминов и пептидных гормонов не могут не затронуть функции высшей нервной деятельности, и, действительно, у пациентов с НЭО часто фиксируются расстройства нервно-психического статуса 6.
Тяжелым проявлением НЭО является карциноидный криз. Он характеризуется интенсивно выраженными признаками: нарушениями ЦНС вплоть до потери сознания и комы, сердечно-сосудистыми расстройствами, включающими аритмии, артериальную гипертензию или гипотензию 5.
НЭО червеобразного отростка среди всех НЭО занимает особое место. Частота постановки этого диагноза составляет 0,15 случая на 100 тыс. населения в год. Болеют преимущественно женщины. Средний возраст больных – 40-50 лет. НЭО червеобразного отростка выявляются, как правило, случайно, во время аппендэктомии (каждый 3-5-й случай на 1 тыс. аппендэктомий). Пятилетняя выживаемость при местнораспространенном новообразовании составляет 85-100%, при распространенной форме – 25% [7].
Исходя из этих данных можно сделать вывод: НЭО червеобразного отростка размерами менее 1 см, без распространения в мезоаппендикулярную область, с четкими контурами, даже после простой аппендэктомии не рецидивируют, в то время как в отношении опухолей более 2 см, с инвазией в мезоаппендикулярную область, существует большой риск развития рецидивов после простой аппендэктомии – требуется проводить правостороннюю гемиколэктомию [7].
Мы приводим клинический случай больной в возрасте 65 лет с диагнозом «НЭО червеобразного отростка». В клинике выполнено хирургическое лечение данной пациентки. Больная была социально адаптирована.
Клинический случай
Пациентка Л., 65 лет, поступила в проктологическое отделение КУ «ХГКБ им. Е.Е. Карабелеша» 19.12.2014 г. с жалобами на боли в правой подвздошной области (в проекции слепой кишки), запоры – в течение 3-4 дней, приливы c гиперемией кожи лица и шеи 2 раза в неделю.
Anamnesis morbi: В 2007 г. пациентка находилась на лечении в гастротерапевтическом отделении; по данным эпикриза, при пальпации в правой подвздошной области выявлялась плотноэластической консистенции слепая кишка, а по данным УЗИ органов брюшной полости (ОБП), в правой подвздошной области – гипоэхогенное образование 3,3×1,3 см.
Из вышесказанного можно сделать вывод, что на то время НЭО имела место и медленно развивалась.
Со слов пациентки, 2-3 раза в неделю у нее наблюдались «приливы» с гиперемией кожи лица, которые она связывала с последствием перенесенной в 1994 г. операции (надвлагалищной ампутации матки с придатками).
Пациентка не обращалась к докторам вплоть до появления у нее в 2014 г. выделений из влагалища. Гинеколог направила больную на УЗИ органов малого таза (ОМТ), где в проекции червеобразного отростка был выявлен фрагмент кишки размером 3,9×1,9 см с утолщенными стенками, частичной потерей физиологической слоистости, пузырьками воздуха в просвете. Вероятнее всего, описанное образование является мукоцеле червеобразного отростка.
После УЗИ пациентку проконсультировал хирург, который исключил острый аппендицит и направил больную на консультацию к проктологу.
На осмотре у проктолога 11.12.2014 г.: в проекции аппендикса на УЗИ ОБП выявлены патологические изменения (см. описание выше). По данным фиброколоноскопии 10.12.2014 г. – за илеоцекальным клапаном нечетко определяется локальное выпячивание стенки за счет сдавливания извне. Слизистая в области площадки устья червеобразного отростка не изменена.
В анамнезе – экстирпация матки с придатками по поводу миомы 20 лет назад и холецистэктомия. Жалобы на приливы в течение 20 лет, боли в правой подвздошной области примерно 1 год. Общий анализ крови: Hb – 130 г/л, СОЭ – 7 мм/ч. В правой подвздошной области пальпируется плотное, умеренно болезненное образование, бугристое, ограниченно подвижное, размерами 4,0×5,0 см. Можно предположить наличие патологии червеобразного отростка, включая НЭО. Показано: осмотр через 1 нед; при сохранении жалоб – оперативное лечение.
18.12.2014 г. Пациентка обратилась повторно с теми же жалобами. Показана госпитализация, оперативное лечение после дообследования с повторным УЗИ ОБП – осмотр тканей вокруг подвздошных сосудов, мочеточника, забрюшинного пространства.
19.12.2014 г. Госпитализирована в проктологическое отделение для дообследования и оперативного лечения с диагнозом: «Объемное образование правой подвздошной области; НЭО червеобразного отростка?».
В anamnesis vitae обращает на себя внимание тот факт, что менопауза у пациентки имеет место 20 лет. Сестра и мать умерли от рака грудной железы.
При поступлении: масса тела – 59 кг, рост – 155 см. Общее состояние удовлетворительное. АД 120/80 мм рт. ст. Пульс 70 уд/мин. Кожа и видимые слизистые бледно-розового цвета, без высыпаний, чистые. Периферические лимфатические узлы не пальпируются.
Status localis: В правой подвздошной области при глубокой пальпации определяется бугристая опухоль 4×5 см малоподвижная, с нечеткими контурами, плотной консистенции.
Клинический диагноз: объемное образование правой подвздошной области; НЭО червеобразного отростка?
Лабораторно-инструментальные исследования провели по стандарту. Из особенностей нужно отметить следующие.
УЗИ ОБП совместно с лечащим врачом от 22.12.2014 г. В проекции правой подвздошной области выявлено новообразование овальной формы с неровным контуром размерами до 3,5×1,5 см низкой эхогенности и умеренной локальной болезненности, вероятно, расположенное вне просвета кишечника (детализация затруднена).
Данные клинико-инструментального обследования не позволяют произвести 100% верификацию заболевания. Показано оперативное лечение, объем которого будет определен после ревизии ОБП.
После подготовки пациентке 24.12.2014 г. выполнена операция – резекция илеоцекального угла кишечника с илеоасцендоанастомозом «конец в конец», рассечение спаек.
В брюшной полости массивный плоскостной спаечный процесс. При ревизии выявлено опухолевидное образование в илеоцекальном углу кишечника, точнее, в его брыжейке при отсутствии червеобразного отростка с деформацией купола слепой кишки в месте его основания. Опухоль бугристая, костной плотности размерами 5,0×1,5 см, интимно сращена с брыжейкой терминального отдела подвздошной кишки. Сам отросток визуально не определяется, расположен за слепой и восходящей кишкой в брыжейке. Выделить его из сращения без нарушения кровоснабжения подвздошной кишки нельзя. Состояние расценено как хронический аппендикулярный инфильтрат с оссификацией червеобразного отростка. В отношении НЭО отростка есть большие сомнения. Из-за нарушения проходимости в илеоцекальном клапане и наличия до конца неясной этиологии измененного червеобразного отростка была выполнена резекция илеоцекального угла кишечника с удалением 15 см подвздошной кишки и ее брыжейки, слепой и восходящей кишки с перевязкой подвздошно-ободочных сосудов и наложением асцендоилеоанастомоза конец в конец. Проходимость анастомоза хорошая.
Перитонизация. Произведены туалет брюшной полости и послойное ушивание раны наглухо.
Макропрепарат (описание). 1. Илеоцекальный угол: 7 см подвздошной кишки, 6 см слепой – с червеобразным отростком. Червеобразный отросток представляет собой конгломерат, спаянный с брыжейкой толстой кишки, на разрезе с участком костной плотности, на разрезе просвет облитерирован, стенка неравномерно утолщена, с участками кальциноза. В подлежащей жировой ткани – округлое образование без границ диаметром 1,5 см. Остальные стенки толстой кишки и тонкой кишки без особенностей + прилежащая жировая клетчатка.
2. Серо-желтый фрагмент 2×1,5 см, на разрезе среди жировой клетчатки отмечается белесоватый фрагмент размером 1 см в диаметре – лимфоузел (?) (рис. 1).
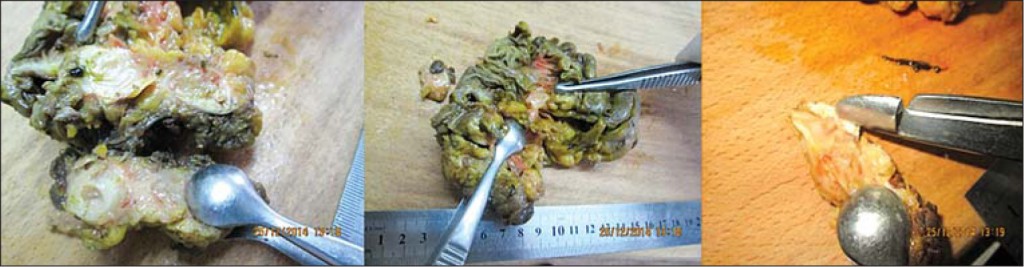
Рис. 1. Макропрепарат

Рис. 2. Морфологическое исследование биопсийного материала A. Карциноид толстой кишки: гнездные скопления имеют типичный внешний вид эндокринных маленьких, округлых клеток с круглым ядром. B. Карциноид толстой кишки: инвазии опухоли в прилежащую жировую ткань (указано стрелками). C. Карциноид толстой кишки: тубулярные и трабекулярные участки, солидные поля.
Гистологическое исследование материала № 1896 от 25.12.2014 г.: Злокачественный карциноид червеобразного отростка с ростом опухоли в прилежащую жировую ткань, участки кальциноза. № 1894,4 – Контрольные полоски без признаков опухолевого роста. № 1895,2 – Лимфатичеcкий узел с метастазом злокачественного карциноида.
Для решения вопроса о тактике дальнейшего лечения пациентки произведено иммуногистохимическое исследование гистопрепаратов в ООД (маркеры хромогранин А и синаптофизин, маркер пролиферации Ki-67).
Иммуногистохимическое исследование материала № 11 от 26.01.2015 г.: Chromogranin A (SP 6) – положительная реакция, synaptophysin (SP 11) – положительная реакция, Ki-67 (SP 6) – менее 2%.
С учетом морфологической картины и результатов иммуногистохимического исследования опухолевая ткань соответствует НЭО червеобразного отростка с низким потенциалом злокачественности G1.
На 12-е сутки сняты швы. Заживление первичным натяжением. Пациентка выписана в удовлетворительном состоянии. Больной даны рекомендации по дальнейшему наблюдению (специальное лечение не показано).
Заключение
НЭО червеобразного отростка занимают первое место по частоте (80%) среди всех НЭО ЖКТ.
Первичные карциноиды клинически проявляются лишь в 5-10% случаев, при метастазах в печень карциноидный синдром отмечается у 40-45% (до 95%) пациентов, в 50% случаев при поражении гонад, в 20% – при локализации в поджелудочной железе, у 20-30% больных с илеоеюнальной локализацией опухоли, у 5% – с карциноидом легких.
Предварительный диагноз НЭО может быть поставлен на основании клинической картины и обычного гистологического исследования, а окончательная верификация проводится при помощи иммуногистохимического исследования.
При постановке диагноза, выборе алгоритма лечения нужно руководствоваться Клиническими рекомендациями ESMO по диагностике, лечению и наблюдению пациентов при нейроэндокринных гастроэнтеропанкреатических опухолях.
В обязательном порядке нужно проводить лекции для врачей по НЭО для большей онконастороженности при данной патологии.
В Украине существует много проблем, связанных с диагностикой и лечением НЭО. Прежде всего это отсутствие национального регистра по учету НЭО или хотя бы приблизительных данных о распространенности патологии. В настоящее время нейроэндокринный рак включен в общую статистику злокачественных новообразований по органной принадлежности. Другими словами, в национальном регистре злокачественных опухолей нет диагноза «нейроэндокринная опухоль». Такое положение препятствует распространению знаний о НЭО среди врачей-онкологов в регионах. Также отсутствуют образовательные программы по патоморфологической, рентгенологической диагностике и терапии НЭО. Большинство патологоанатомических и биохимических лабораторий не располагают возможностями для диагностики НЭО, поэтому об опыте лечения вообще говорить не приходится. Новые препараты, эффективность которых при НЭО была доказана в международных клинических исследованиях, длительное время проходят регистрацию в Украине, что также ограничивает возможности терапии НЭО на современном уровне.
Литература
1. Obendorfer S. Karzinoide tumoren des Dunndarms // Frankf. Z. Pathol. 1907. Vol. 1. P. 425-429.
2. Niederle M.B., Hackl M., Kaserer K. et al. Gastroenteropancreatic neuroendocrine tumours: the current incidence and staging based on the WHO and European Neuroendocrine Tumour Society
classification: an analysis based on prospectively collected parameters. Endocr Relat Cancer 2010; 17: 909-918.
3. Yao J.-C. One hundred years after «carcinoid»: epidemiology of and prognostic factors for neuroendocrine tumors in 35,825 cases in the United States / J.-C. Yao, M. Hassan, A. Phan et al. // J Clin Oncol 2008. – 26. – P. 3063-3072.
4. Barakat M.T. Neuroendocrine tumors. / M.T. Barakat, K. Meeran, S.R. Bloom // Endocrin. Relat. Cancer. – 2004. – 11. – P. 1-18.
5. Jensen R.T. Carcinoid Tumors and the Carcinoid Syndrome / R.T. Jensen, J.M. Doherty // Cancer: Principles and Practice of Oncology. – 2000. – Ch. 38.6.
6. Kulke M.H. Neuroendocrine tumours: clinical presentation and management of localized disease /
M.H. Kulke // Cancer Treat. Rev. – 2003. – Vol. 29. – P. 363-370.
7. ENETS Consensus Guidelines for the Management of Patients with Neuroendocrine Neoplasms from the Jejuno-Ileum and the Appendix Including Goblet Cell Carcinomas – Р. 143-152.
СТАТТІ ЗА ТЕМОЮ Ендокринологія
Похідні сульфонілсечовини є поширеними пероральними цукрознижувальними засобами в країнах із низьким і середнім рівнями доходу. Крім того, наразі відсутня уніфікована позиція цієї групи препаратів у національних та міжнародних рекомендаціях. Метою цього огляду було оцінити різні національні та міжнародні рекомендації щодо лікування ЦД 2 типу, що дозволить ефективніше й безпечніше їх застосовувати в різних клінічних ситуаціях.
Під час міжнародного конгресу ATTD у квітні 2022 року було анонсовано результати клінічного дослідження InRange – першого рандомізованого контрольованого міжнародного дослідження для порівняння аналогів базального інсуліну II покоління гларгін‑300 (Гла‑300) та деглюдек‑100 (ІДег‑100) у пацієнтів із цукровим діабетом (ЦД) 1 типу з використанням часу в цільовому діапазоні глікемії (TIR) як первинної кінцевої точки. Первинною метою дослідження було довести не меншу ефективність Гла‑300 проти ІДег‑100 у досягненні TIR у пацієнтів із ЦД 1 типу, які раніше отримували базальні аналоги інсуліну I покоління та аналоги інсуліну короткої дії. .
Від 24 лютого життя мешканців нашої країни докорінно змінилося. Усі ми стали свідками суворої та небезпечної реальності, сповненої невизначеності й обмежень. Особливо складно людям із хронічними захворюваннями, котрі мають неабиякі труднощі внаслідок обмеження доступу до якісних препаратів і медичної допомоги загалом. Нині в складних економічних умовах такі хворі потребують призначення недорогого й водночас якісного та безпечного лікування. Про проблеми, з якими стикнулися пацієнти із цукровим діабетом (ЦД) 2 типу під час бойових дій, і про можливості їх вирішення в рамках вебінару, організованого освітньою платформою «Аксемедін», розповіла доцент кафедри ендокринології Львівського національного медичного університету ім. Данила Галицького, кандидат медичних наук Христина Андріївна Москва.
Аналоги базального інсуліну ІІ покоління мають значні переваги в застосуванні в хворих на цукровий діабет (ЦД), оскільки характеризуються тривалішим ефектом, сприятливішим фармакокінетичним профілем і забезпечують менші добові коливання рівня глікемії. Утім, і досі не було проведено прямого порівняння між безпекою та ефективністю цих препаратів в осіб із ЦД 1 типу. .
Опухоли толстой и прямой кишки

Опухоли толстого кишечника
Опухоли толстого кишечника — это доброкачественные либо злокачественные новообразования разной этиологии, которые развиваются из эпителиальной или другой ткани стенок толстой кишки и могут поражать любые ее отделы. Доброкачественные опухоли довольно распространены, по разным данным они выявляются у 16−40% населения. Во многих случаях доброкачественный процесс со временем переходит в злокачественный. Раковые опухоли толстого кишечника занимают третье место среди другой злокачественной патологии пищеварительной системы (после рака желудка и опухолей пищевода).
Среди всей онкопатологии злокачественные опухоли толстого кишечника по частоте уступают только раку легких, раковым новообразованиям в желудке и раку молочной железы. У мужчин заболевания данной группы, особенно злокачественные, выявляют несколько чаще, нежели у женщин. Актуальность опухолей толстого кишечника возрастает с каждым годом, преимущественно в развитых странах северного полушария. Доброкачественные процессы так же опасны, как и злокачественные, поскольку имеют склонность к малигнизации.
Причины опухолей толстого кишечника
Причины, которые приводят к возникновению опухолей толстого кишечника, изучаются давно, но к единому мнению ученые и клиницисты (проктологи, хирурги) так и не пришли. Все сходятся во мнении, что данная группа заболеваний является полиэтиологичной. Риск формирования патологии повышается с возрастом. Большое значение имеет диета, богатая животными белками, жирами и бедная клетчаткой. Такой рацион ведет к частым запорам, дисбалансу кишечной флоры. Содержимое кишечника с высоким содержанием желчных кислот и фенолов, обладающих канцерогенными свойствами, дольше контактирует со стенками, что повышает возможность развития опухолей толстого кишечника. Именно с этим связывают большее распространение опухолей толстого кишечника в развитых странах. Также имеют значение канцерогены, которые содержатся в промышленных консервантах, копченых продуктах.
Немаловажное значение в возникновении опухолей толстого кишечника, как злокачественного, так и доброкачественного характера, имеют воспалительные заболевания. При длительном течении (пять лет и больше) они могут осложняться раком
Классификация опухолей толстого кишечника
Опухоли толстого кишечника делят на доброкачественные и злокачественные, а также на опухоли эпителиального и неэпителиального происхождения. По международной морфологической классификации выделяют следующие эпителиальные доброкачественные опухоли толстого кишечника:
Эпителиальные опухоли самые распространенные, они составляют около 92% всех новообразований, имеют большую склонность к злокачественному перерождению.
Злокачественные опухоли толстого кишечника по характеру роста разделяют на четыре типа:
экзофитно-полиповидные опухоли, которые растут в просвет кишки;
эндофитно-язвенные опухоли, распространяющиеся в стенке кишки, часто дают изъязвления;
диффузно-инфильтративные опухоли (злокачественные клетки имеют диффузное распространение внутри стенок органа);
аннулярные опухоли — растут по окружности кишки.
В двух последних случаях трудно определяются гистологические границы опухолевого процесса, клетки могут проникать в участки, которые на первый взгляд выглядят здоровыми.
При классификации злокачественных опухолей толстого кишечника большое значение имеет стадия процесса. Стадийность определяют с помощью международной общепринятой классификации TNM, где T — это степень прорастания опухоли в ткани, N — наличие или отсутствие метастазирования в регионарные лимфатические узлы, M — отдаленное метастазирование.
Симптомы опухолей толстого кишечника
Доброкачественные опухоли толстого кишечника часто протекают бессимптомно и выявляются случайно. Иногда у больных появляется дискомфорт в животе, неустойчивый стул или кровь в кале.
Раковые опухоли толстого кишечника развиваются достаточно медленно и в самом начале могут клинически не проявляться. Одними из первых симптомов заболевания являются кровотечения и анемия. При опухолях прямой кишки и нижнего отдела сигмовидной кишки кровь алая, не смешивается со слизью. Если патологический процесс затрагивает начальную ободочную кишку — кровь темная, равномерно перемешанная со слизью и калом. Кровотечения при злокачественном процессе в проксимальных отделах очень часто бывают скрытыми и проявляются только анемией.
Кроме кровотечений, при раковых опухолях толстого кишечника у пациентов могут появиться боли в животе, тенезмы, проблемы со стулом. Запоры возникают на поздних стадиях процесса, в запущенных случаях часто развивается кишечная непроходимость. Раковые поражения прямой кишки вызывают у больных ощущение неполного опорожнения, тенезмы. Пациенты жалуются на общую слабость, потерю аппетита, отмечают резкую потерю веса. С прогрессированием болезни увеличивается печень, появляются признаки асцита.
Диагностика опухолей толстого кишечника
Для диагностики опухолей толстого кишечника используют целый ряд методик. При аноскопии и ректороманоскопии обнаруживают опухоли и полипы в прямой кишке, дистальном участке сигмовидной кишки.
После проведения эндоскопии выполняют ирригоскопию с двойным контрастированием путем введения в кишечник воздуха и бариевой взвеси. Методика позволяет выявить опухоли толстого кишечника разного размера; трудности в диагностике могут возникнуть, если процесс локализирован в слепой кишке.
Следующий этап исследования — проведение колоноскопии, которая позволяет выявить небольшие по размеру опухоли толстого кишечника, осмотреть его на всем протяжении. Также с помощью этого метода можно взять биоптат и удалить небольшого размера полипы. Колоноскопия имеет большую чувствительность по сравнению с ирригоскопией, но наиболее достоверные результаты можно получить при использовании эндоскопии и контрастной рентгенографии.
Для выявления метастазов при злокачественных опухолях толстого кишечника используют УЗИ органов брюшной полости, компьютерную томографию, сканирование костной системы, при наличии неврологических симптомов — КТ головного мозга. Опухолевые маркеры имеют скорее прогностическое, чем диагностическое значение. При низкодифференцированных новообразованиях повышается раково-эмбриональный антиген, хотя он не специфичен для этого типа опухолей. Самыми информативными маркерами при выявлении первичных опухолей толстого кишечника считаются маркеры СА-19−9 и СА-50, но при рецидивах они могут и не определяться.
Лечение опухолей толстого кишечника
Единственный действенный метод лечения опухолей толстого кишечника в современной проктологии — хирургический. При небольших доброкачественных процессах без признаков малигнизации проводят удаление новообразования, при множественном поражении — части толстого кишечника.
При злокачественных опухолях толстого кишечника объем операции более радикальный. Удаляют не только новообразование, но и региональные лимфатические узлы, даже если в них не выявлены метастазы. По возможности во время хирургических вмешательств стараются сохранить естественный путь пассажа кишечного содержимого. Если такой возможности нет, выводят колостому на переднюю брюшную стенку. Кроме оперативного лечения, назначают химиотерапию, лучевую терапию.
Прогноз и профилактика опухолей толстого кишечника
Прогноз при опухолях толстого кишечника не всегда благоприятный. Даже доброкачественные эпителиальные опухоли или полипы имеют высокую склонность к злокачественному перерождению. Во многом выживаемость больных зависит от своевременной диагностики и адекватно проведенной хирургической операции.
Профилактика опухолей толстого кишечника состоит, прежде всего, в правильном питании. Необходимо меньше употреблять копченых и консервированных продуктов, мяса и животных жиров. При выборе продуктов нужно отдавать предпочтение тем, которые содержат большое количество клетчатки. Следует пересмотреть образ жизни: низкая двигательная активность благоприятствует возникновению опухолей толстого кишечника. Необходимо вовремя выявлять и лечить различные воспалительные заболевания желудочно-кишечного тракта.
Пальпация слепой кишки
Пальпация слепой кишки. Пальпируется у 78—85% людей, в правой подвздошной области. Ее длинник располагается косо (справа сверху вниз и влево) на границе средней и наружной трети линии, соединяющей пупок и правую верхнюю переднюю ость подвздошной кости.

Рис. 55. Пальпация:
а, б — сигмовидной кишки соответственно четырьмя пальцами и локтевым краем мизинца;
в, г — соответственно слепой и подвздошной кишки.
Техника пальпации слепой кишки (рис. 55, в) аналогична таковой при пальпации сигмовидной кишки. Слепую кишку пальпируют четырьмя полусогнутыми сложенными вместе пальцами правой руки. Их устанавливают параллельно длиннику кишки. Поверхностным движением пальцев по направлению к пупку создают кожную складку. Затем, постепенно погружая пальцы в брюшную полость, во время выдоха доходят до задней брюшной стенки, скользят по ней, не разгибая пальцы, перпендикулярно кишке, по направлению к правой передней ости подвздошной кости и перекатываются через слепую кишку. Если ее пропальпировать сразу не удалось, пальпацию следует повторить. При этом стенка слепой кишки из расслабленного состояния под влиянием раздражения переходит в состояние напряжения и уплотняется (из-за сокращения мышечного слоя кишки). При напряжении брюшного пресса можно тенаром и большим пальцем свободной левой руки надавить около пупка на переднюю брюшную стенку и продолжить исследование слепой кишки пальцами правой руки. Этим приемом напряжение брюшной стенки в области слепой кишки переносится на соседнюю.
В норме слепая кишка прощупывается в форме гладкого, безболезненного, слегка урчащего цилиндра, шириной 3—5 см, умеренно упругого и слабо подвижного, с небольшим грушевидным расширением книзу. Подвижность слепой кишки в норме составляет 2—3 см. При чрезмерной подвижности ее могут наблюдаться приступы внезапных болей с явлениями частичной или полной непроходимости вследствие перегибов и заворотов. Уменьшение подвижности кишки или полная ее неподвижность могут быть вызваны спайками, возникшими после перенесенного воспалительного процесса в этой области.
Слепая кишка больше, чем сигмовидная, подвержена разным изменениям. Консистенция, объем, форма, болезненность при пальпации и акустические феномены (урчание) слепой кишки зависят от состояния ее стенок, а также от количества и качества содержимого. Болезненность и громкое урчание при пальпации слепой кишки наблюдаются в случае воспалительных процессов в ней и сопровождаются изменением ее консистенции. При некоторых заболеваниях (туберкулез, рак) кишка может приобретать хрящевую консистенцию и становится неровной, бугристой и малоподвижной. Объем кишки зависит от степени наполнения ее жидким содержимым и газом. Он увеличивается при скоплении каловых масс и газов в случае запоров и уменьшается при поносах и спазме ее мускулатуры.
Читайте также:
