Эффективность операций при хронической эмпиеме плевры. Биопсия в торакальной хирургии
Обновлено: 25.04.2024
Заболевание пищевода, сопровождающееся воспалением его слизистой оболочки.
Диагностика:
- эзофагогастродуоденоскопия;
- эзофагогастродуоденоскопия с биопсией.
Тромбозы и эмболии артерий - внезапная закупорка магистральных сосудов. Мгновенное прекращение доставки крови к органу приводит к гибели органа и запускает механизмы, приводящие к гибели всего организма. Тромбозом магистральной артерии называется образование тромба на измененной стенке артерии с закупоркой просвета сосуда. Основной причиной тромбоза является атеросклероз при котором изменение сосудистой стенки ведет к турбуленции крови, склеиванию эритроцитов и тромбоцитов и оседанию их на стенке. Эмболия это перенос током крови организованного тромба из другой области (сердца или аорты) в другой сосуд и закупоркой его.
Наиболее часто эмболии случаются при болезнях сердца (инфаркт миокарда, мерцательная аритмия, инфекционное поражение сердечных клапанов) и при расширении крупных сосудов - аневризмах. При попадании его в мозговые сосуды развивается инсульт, в кишечник - мезентериальный тромбоз, в руку или ногу - гангрена. При тромбозе или эмболии, нормальное кровоснабжение в бассейне закупоренного сосуда внезапно прекращается и развивается патологическое состояние называемое острой ишемией. При ишемии кислородный голод приводит к прекращению функционирования, а в последующем, и гибели тканей пораженного органа. Выключение функции начинается с нервной ткани. При этом вначале происходит ее раздражение, что приводит к сильной боли, затем прекращается проведение нервного импульса - исчезает чувствительность, конечность "деревенеет". В итоге развивается паралич мышц - активные движения прекращаются.После гибели нервной ткани наступает умирание мышечной ткани. Этот процесс сопровождается окоченением отдельных мышц и их групп с развитием тугоподвижности суставов, а в последующем и невозможности согнуть конечность ни в одном суставе.
Подобное состояние называется мышечной контрактурой. Наиболее жизнеспособна кожа. Нередко приходилось наблюдать полную гибель мышц, тогда как кожа внешне остаётся не измененной. Полная мышечная контрактура свидетельствует о гибели конечности и необходимости срочной ее ампутации с целью спасения жизни, так как всасывание продуктов мышечного распада приводит к необратимому отравлению организма с нарушением функции всех жизненно-важных органов. Процесс развития острой ишемии достаточно быстрый, но на определенных этапах обратимый. Если орган или конечность утратили свою функцию, но еще не погибли, то восстановление кровообращения дает шанс полного их восстановления. В поздние сроки восстановление может быть неполным, потеря времени лишает всякой надежды.
Срок, отпущенный острой ишемией для существования конечности, зависит от многих факторов. При тромбозе гибель конечности наступает не сразу и не всегда, так как сосуд был изначально сужен атеросклеротической бляшкой, а конечность привыкла вести "полуголодное" существование. Развивались окольные пути кровоснабжения. Однако изменение условий кровоснабжения углубляет дефицит кислорода и постепенно приводит к умиранию органа.
При тромбозах в зависимости от объема и жизненной важности органа есть 2-5 дней для спасения. При эмболиях нарушение кровоснабжения наступает мгновенно, что приводит к резкому спазму артерий и выключению коллатерального кровообращения. Отсутствие доставки кислорода к органу или конечности запускает механизмы острой ишемии. При эмболиях лучшие результаты лечения для восстановлении кровотока в головном мозге минуты, внутренних органах от 30 минут до 1 часа, конечностях до 6 часов, от начала заболевания. До 12 часов можно спасти только 60% конечностей, после 24 часов лишь 20 %. Боль при недостаточности крови возникает в начале болезни. При эмболии боль сильнее и напоминает удар и бывает очень сильной. При тромбозах болевые ощущения менее выражены и часто характеризуются "нога затекла, онемела". Постепенно болевые ощущения затихают, что связано с гибелью нервных окончаний. Второй основной признак - изменение окраски кожных покровов и резкое снижение температуры конечности. Она становится "ледяной" на ощупь. При эмболии чаще вначале кожа резко бледнеет, затем по мере уменьшения боли начинает синеть, становится "мраморной". Следующим этапом исчезает чувствительность. При этом сохраняется чувство тупой боли, но покалывание иглой, прикосновение горячим и холодным не ощущается. Вслед за исчезновением чувствительности исчезают и движения. Пораженная конечность не воспринимается, как своя, но пассивные движения еще возможны. Этот этап является последним, когда еще можно восстановить функцию конечности. В дальнейшем развивается отек мышц, частичная и полная мышечная контрактура.
От скорости обращения больного к сосудистому хирургу зависит исход лечения. Ни в коем случае нельзя согревать больную конечность. В стационаре при эмболии в ближайшие часы сделают экстренную операцию по извлечению тромбов (эмболэктомию). При тромбозе часто есть несколько дней для обследования. Производятся операции шунтирования или протезирования закупоренного участка сосуда. Для исключения таких состояний любые боли или неприятные ощущения в конечностях должны стать поводом к обращению за консультацией сосудистому хирургу.
Эмпиема плевры – воспаление плевральных листков с накоплением гноя между ними. По характеру возбудителя воспаления различают специфическую (туберкулезную, актиномикотическую) и неспецифическую эмпиему плевры. Среди возбудителей неспецифической эмпиемы плевры превалируют стафилококки, стрептококки, протей, синегнойная палочка, кишечная палочка, которые преимущественно находятся в ассоциации с неклостридиальной анаэробной микрофлорой (более чем в 50% случаев): фузобактериями, бактероидами, пептококками, пептострептококками.
Различают первичную и вторичную эмпиему плевры. На практике чаще встречается вторичная, которая является осложнением какого-либо другого гнойного воспаления – пневмонии, абсцесса или гангрены легкого, остеомиелита ребер, медиастинального лимфаденита. При первичной эмпиеме плевры инфекция попадает в плевральную полость при травме груди, резекции легких, реже гематогенно при сепсисе.
Классификация эмпием плевры.
По клиническому течению:
- острые (до 3 месяцев);
- хронические (свыше 3 месяцев).
По наличию деструкции легкого:
- эмпиема без деструкции легкого (простая);
- эмпиема с деструкцией легкого;
- пиопневмоторакc.
- Закрытые.
- Открытые:
- с бронхоплевральным свищем;
- с плеврокожным свищем;
- с бронхоплевральнокожным свищем;
- с решетчатым легким;
- с другим полым органом.
- ограниченные (чаще осумкованные спайками);
- субтотальные;
- тотальные.
Клиническая картина.
Клинические проявления острой эмпиемы зависят от распространенности гнойного процесса, вирулентности микрофлоры, степени деструкции легочной ткани, реактивности больного, а также от своевременности и полноценности проводимого лечения (Рис. 2.3.). В большинстве случаев заболевание протекает на фоне дыхательной и сердечно-сосудистой недостаточности, которые обусловлены полным или частичным спадением легкого, смещением средостения, сдавлением крупных сосудов и нарастающей эндогенной интоксикацией.
При объективном обследовании отмечается бледность кожи и слизистых оболочек, тахикардия, одышка. Грудная клетка на стороне поражения становится бочкообразной со сглаженными межреберьями. Перкуторно отмечается притупление легочного звука в нижних отделах и коробочный звук выше горизонтальной линии жидкости. Аускультативно – резкое ослабление или отсутствие дыхательных шумов. При закрытой эмпиеме, при отсутствии воздуха в плевральной полости и сращений, верхняя граница тупости соответствует линии Эллиаса-Дамуазо, а над зоной тупости отмечается тимпанический звук (признак Шкоды).
Диагностика.
Рентгенологически на стороне эмпиемы определяется интенсивное затенение, смещение средостения в здоровую сторону. При пиопневмотораксе верхняя граница жидкости становятся горизонтальной. Над уровнем жидкости определяется воздушная полость. В зависимости от степени коллапса легкого различают ограниченный, субтотальный и тотальный пиопневмоторакс. При ограниченных эмпиемах плевры для уточнения формы, размеров, наличия бронхиальных свищей проводят плеврографию – введение водорастворимых контрастных веществ в полость эмпиемы с помощью пункции или через фистулу при наличии плеврокожного свища.
В последние годы в диагностике острых и хронических эмпием плевры все большее распространение получает ультразвуковое исследование, особенно при осумкованных, ограниченных эмпиемах, когда скопления жидкости маскируются массивными плевральными швартами и оказываются недоступными для рентгенологического распознавания. В ряде случаев при отграниченной гнойной полости возможно выполнение пункции и дренирования ее под контролем ультразвука. В трудных для диагностики ситуациях в первую очередь для выявления деструкции в легком используют компьютерную томографию.
Одним из обязательных этапов диагностики эмпиемы плевры является диагностическая пункция плевральной полости. Она позволяет окончательно установить этиологическую причину накопления выпота в плевральной полости – геморрагический при раке легкого, гной при туберкулезе, актиномикозе, неспецифической эмпиеме. Цитологическое, биохимическое и бактериологическое исследования содержимого плевральной полости является обязательным.
Лечение эмпиемы плевры включает:
1. Полноценную аспирацию гноя и санацию плевральной полости, которые при ограниченных эмпиемах достигаются регулярными пункциями, аспирациями гноя, промываниями полости эмпиемы антисептиками и введением антибиотиков; при открытых, тотальных и субтотальных эмпиемах – дренированием и промыванием полости эмпиемы.
2. Мероприятия, направленные на скорейшее расправление легкого (дренирование с активной аспирацией, при наличии бронхиального свища – с временной окклюзией бронха, или дренирование по Бюлау).
3. Массивную антибактериальную терапию (цефалоспорины III-IV поколения, фторхинолоны, карбапенемы).
6. Общеукрепляющую терапию, направленную на восстановление функций жизненно важных органов и систем.
Возможны следующие основные варианты санации плевральной полости: пассивное дренирование с фракционным лаважем; постоянная активная аспирация с фракционным лаважем или непрерывное промывание полости. Однако наиболее эффективным приемом лечения острой эмпиемы плевры является фракционный лаваж или непрерывное промывание полости в сочетании с активной аспирацией. Точку для пункции или дренирования полости плевры определяют на основании многоосевой рентгеноскопии. Сроки нахождения дренажной трубки в плевральной полости во многом зависят от быстроты расправления легкого и прекращения отделения гноя, но в среднем составляют 2-3 недели.
При лечении эмпиемы плевры отсасывают по возможности весь экссудат. При наличии густого гноя, пленок фибрина или казеозных масс применяют протеолитические ферменты, способствующие разжижению вязкого гноя, лизису напластований фибрина на плевральных листках и потенцирующему действию антибиотиков. Наряду с ферментами в полость плевры вводят растворы антибиотиков, которые подбирают с учетом характера и чувствительности выделенной из экссудата микрофлоры. У больных с острым гнойным плевритом такое лечение обычно уже через 2-3 недели приводит к прекращению накопления экссудата в плевральной полости, улучшению общего состояния, ликвидации явлений интоксикации и в конечном итоге к выздоровлению.
Если не удается добиться облитерации полости и расправления легкого, формируется хроническая эмпиема плевры. В этих случаях единственно эффективным методом лечения является оперативное вмешательство – плеврэктомия с декортикацией легкого, а при наличии деструкции в легком, бронхоэктазов – резекция легкого.
Эффективность операций при хронической эмпиеме плевры. Биопсия в торакальной хирургии
Эффективность операций при хронической эмпиеме плевры. Биопсия в торакальной хирургии
Ближайшая эффективность выполненных нами оперативных вмешательств оказалась следующей: хороший клинический эффект достигнут у 106 больных (91,3%), удовлетворительные результаты — у 4 (3,5%). Выписан с осложнением один больной (0,9%) и умерло—5 (4,3%).
Отдаленные результаты в сроки от 2 до 9 лет прослежены у 95 больных. Полное клиническое выздоровление установлено у 86 обследованных (90,5%), удовлетворительные результаты— у 8 (8,4%), умер—один больной (1,1%). Причинами отдаленных удовлетворительных результатов служили реактивация туберкулезного процесса в легком и легочно-сердечная недостаточность.
Одним из объективных критериев эффективности операций является стойкое восстановление трудоспособности. Вопросы трудовой реабилитации после плеврэктомии изучены нами у 55 больных. Хроническая эмпиема плевры служила причиной временной нетрудоспособности до 6 месяцев у 27 больных, свыше 6 месяцев — у 23, инвалидами I, II, III групп были 5 больных.
После плеврэктомии в сроки от 4 до 8 месяцев приступили к выполнению своей прежней профессии 39 человек, а через 1—2 года — еще 14. Всего в отдаленные сроки после операции трудоспособность была восстановлена у 53 человек из 55 обследованных (96,3%)- Приступили к более легкой работе, не сопряженной со значительным физическим напряжением, 7 человек (12,7%). Следовательно, плеврэктомия в реабилитационном отношении также является высокоэффективной, что имеет большое социально-экономическое значение.
Таким образом, наши клинические наблюдения убедительно свидетельствуют о том, что в современных условиях плеврэктомия в сочетании с резекцией легкого или без нее у больных с хронической эмпиемой плевры является основным и высокоэффективным методом хирургического лечения.

Биопсия в торакальной хирургии
В настоящее время благодаря широкому применению флюорографии, совершенствованию рентгенологических методов исследования, многие патологические процессы в легких, бронхах, средостении, плевре выявляются уже на ранних стадиях. С другой стороны, рентгенологическое выявление патологии не всегда означает установление диагноза. Это обусловлено объективными трудностями, так как сходная рентгенологическая картина нередко является отражением различных заболеваний.
Достаточно часто встречаются случаи, когда заболевание протекает стерто, атипично или не является характерным для данной возрастной группы и, вследствие этого, лечение проводится неправильно или больной остается под наблюдением без лечения.
И если при некоторых заболеваниях, например, при эозинофильном инфильтрате или бронхопневмонии запоздалое установление правильного диагноза существенно не влияет на прогноз, то при раке, туберкулезе судьба больного нередко зависит от того, насколько своевременно была определена этиология патологического процесса. Установление природы заболевания по данным стандартного обследования (анамнез, клиника, рентгенологические, лабораторные данные) во многих случаях оказывается затруднительным или даже невозможным из-за значительного сходства клинико-рентгенологических проявлений при многих заболеваниях.
Ведущие пульмонологи нашей страны в последние годы настоятельно пропагандируют необходимость ранней диагностики при заболеваниях органов дыхания, применение активных методов исследования для установления этиологии интраторакальных патологических процессов (Л. К. Богуш, 1966, 1971, 1973; В. А. Климанский с соавт. 1967; Г. И. Лукомский, 1968; Г. И. Лукомский и М. Л. Шулутко, 1971; А. И. Савицкий, 1967; В. П. Филиппов, 1970; Б. Е. Петерсон, 1971; Г. Г. Горовенко, 1971; В. И. Стручков и С. В. Лохвицкий, 1972; В. И. Стручков, 1973 и др.).
Необходимость применения таких методов исследования подтверждается статистическими исследованиями о частоте и причинах диагностических ошибок у больных с интраторакальными поражениями при использовании стандартных методов исследования (М. И. Тараненко и Л. С. Вайнер, 1970; Г. И. Розенберт с соавт. 1971; М. З. Сорокин и Р. Э. Коган, 1970, М. М. Воропаев и А. А. Адамян, 1971). По данным этих авторов процент диагностических ошибок колеблется от 28 до 86!
- Вернуться в оглавление раздела "Хирургия"
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Эффективность операций при хронической эмпиеме плевры. Биопсия в торакальной хирургии
Лечение неспецифических воспалительных и гнойно-деструктивных заболеваний легких и плевры остается актуальной проблемой торакальной хирургии. В последние годы не наблюдается тенденции к снижению тяжелых и осложненных форм заболевания. Наиболее частым осложнением, влияющим на исход заболевания, является эмпиема плевры. У 11-40% больных острая эмпиема плевры переходит в хроническую.
Постоянное совершенствование хирургических методов и внедрение новых технологий позволяют снизить смертность в ранние сроки заболевания. Однако частота неблагоприятных исходов, особенно при тотальных формах эмпиемы плевры, при позднем и неадекватном лечении, а также при наличии тяжелых сопутствующих заболеваний, остается на высоком уровне и достигает 40%, а при распространенных осложненных гангренозных поражениях легких может превышать 70% [1, 5]. Применение традиционных оперативных методов улучшает непосредственные результаты лечения и снижает частоту хронизации процесса, вместе с тем увеличиваются количества послеоперационных осложнений и летальность.
На сегодняшний день видеоторакоскопия прочно вошла в обиход ведущих лечебных учреждений как современный информативный метод диагностики и эффективный способ лечения, в том числе и эмпиемы плевры [10]. Однако до сих пор нет четко разработанного алгоритма и сроков применения торакоскопии в комплексном лечении больных с неспецифической эмпиемой плевры. Не определено место торакоскопии при гангренозных поражениях легких.
Неспецифическая эмпиема плевры
В отделении гнойной торакальной хирургии с 2008 по 2013 г. находились 618 больных с эмпиемой плевры как осложнением неспецифических воспалительных и гнойно-деструктивных заболеваний легких. Средний возраст больных составлял 45 лет. Чаще эмпиема плевры имела парапневмонический характер, в 108 (17,5%) наблюдениях являлась осложнением различных форм легочных деструкций. У 195 (31,6%) больных диагностирована открытая эмпиема плевры со свищами различного характера и локализации. Около трети больных поступили в отделение первично по скорой медицинской помощи, а большинство (73,2%) - переводом из других стационаров, в том числе из торакальных отделений, в тяжелом состоянии со сроками от начала заболевания более 3 нед. У 36 больных тяжелая двусторонняя деструкция легких, чаще с пиопневмотораксом, была проявлением сепсиса. Большинство из них первично поступали с тяжелыми дыхательными нарушениями в непрофильные отделения, где проводилась респираторная поддержка (ИВЛ), что ограничивало возможности комплексного лечения и в осложненных случаях сопровождалось только закрытым дренированием плевральной полости, при этом не всегда адекватным. В последующем больные поступали в наше отделение в более поздние сроки с момента заболевания и наличием внутрибольничных штаммов микробной флоры.
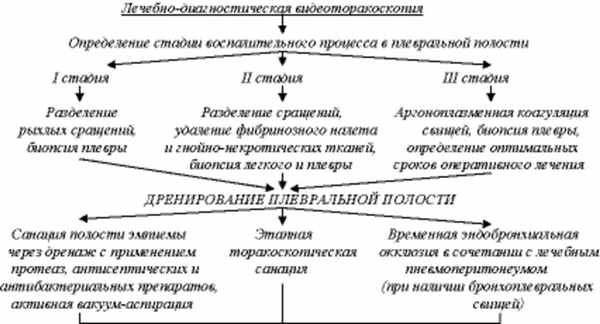
Комплексное лечение включало адекватную санацию полостей деструкции в легких и полости эмпиемы, ликвидацию остаточной внутрилегочной и плевральной полости, этиотропную терапию с обязательным включением в лечебный алгоритм ранних торакоскопических вмешательств (рис. 1). Рисунок 1. Ранняя видеоторакоскопическая санация в алгоритме лечения неспецифической эмпиемы плевры. Определение фазы воспалительного процесса в плевральной полости важно при выборе лечебного алгоритма, особенно при наличии бронхоплевральных свищей и плевролегочных полостей.
По нашему убеждению, любой вариант первичного дренирования плевральной полости по возможности должен сопровождаться торакоскопией («золотой стандарт»). Выполнение торакоскопии в ряде случаев не требует сложного оборудования (видеокамеры, специальных троакаров и т.д.). Преимущества видеоторакоскопии перед прямой торакоскопией, фиброторакоскопией неоспоримы, однако и эти способы осмотра плевральной полости могут предоставить ценную диагностическую информацию и позволяют определить алгоритм всех последующих действий.
Довольно хорошая переносимость больными этой манипуляции под местным обезболиванием (межреберная и паравертебральная блокады) дает возможность раннего применения метода [11]. Ранняя видеоторакоскопия (1-3-и сутки с момента поступления больного в специализированный стационар) является основой для построения лечебно-диагностической программы.
Видеоторакоскопия позволяет оценить характер и распространенность гнойно-деструктивного процесса в легких и плевре, стадию воспалительного процесса, определить локализацию и размеры бронхоплевральных свищей, разделить фибринозные сращения, удалить фибринозный налет с поверхности легкого, плевры и гнойно-некротические ткани из полостей деструкции в легких при наличии плевролегочных полостей, выполнить биопсию, а также (что немаловажно) адекватно дренировать плевральную полость под визуальным контролем, особенно при наличии бронхоплевральных свищей. Биопсию легкого и париетальной плевры выполняли всем больным с целью исключения сочетания неспецифического воспаления с возможным специфическим процессом.
Границы полости и оптимальную точку введения порта для оптической системы определяли при полипозиционной рентгеноскопии, дополненной ультразвуковым исследованием плевральной полости. Торакоцентез выполняли в месте наибольшего расхождения листков париетальной и висцеральной плевры, что позволяло более безопасно ввести первый троакар для оптической системы и имело больший угол обзора остаточной полости. В арсенале оснащения торакоскопическим оборудованием желательно иметь две оптические системы: с прямой и скошенной торцевой оптикой. Применение оптической системы со скошенной оптикой дает возможность осмотреть труднодоступные и так называемые слепые зоны, особенно при ограниченных остаточных полостях, и в случае, когда свободный круговой ход оптической системы ограничивается узкими межреберными промежутками.
Постановку дополнительных манипуляционных портов осуществляли не в предлагаемых стандартных точках, а определяли места введения, исходя из результатов осмотра плевральной полости, конкретного алгоритма дальнейших действий и удобства выполнения манипуляций. По возможности использовали 10-миллиметровый манипуляционный торакопорт, что позволяет менять положение оптической системы с целью полноценного осмотра и адекватной санации полости эмпиемы. Для удобства удаления фибринозного налета и измененной плевры в качестве манипуляционных инструментов использовали набор кюреток с изогнутой под разными углами рабочей частью, которые вводили в плевральную полость без портов.
В отличие от тотальной и субтотальной торакоскопия при ограниченной эмпиеме плевры имеет ряд особенностей, обусловленных малыми размерами и локализацией полости эмпиемы. При малом поперечном размере ограниченной полости для облегчения выполнения и увеличения безопасности торакоцентеза после получения гноя при плевральной пункции вводили в полость эмпиемы раствор антисептика, который отодвигал ткань легкого от места вхождения троакара в плевральную полость. При малых размерах полости эмпиемы торакоскопические манипуляции делали в беспортовом режиме, вводя эндоскопический инструмент вместе с оптикой через один разрез.
Дренирование плевральной полости, как правило, двумя дренажами выполняли через отверстия удаленных портов в верхней и нижней части полости, а при наличии грубых рубцовых сращений легкого с париетальной плеврой - в разных «карманах». Установку дренажей осуществляли под непосредственным визуальным контролем. При наличии бронхоплевральных свищей и ригидном легком обязательным условием была постановка одного из дренажей в самой нижней точке эмпиемной полости. Торакоскопию можно завершить оставлением торакопорта в грудной стенке с фиксацией последнего к коже с целью этапной эндоскопической санации.
В последующем полость эмпиемы промывали во фракционном или проточном режиме с обязательной активной вакуум-аспирацией, по показаниям использовали протеолитические ферменты (террилитин, терридеказа).
Опыт выполнения ранней видеоторакоскопии показывает, что при первой стадии воспалительного процесса в плевральной полости достаточно адекватного дренирования полости эмпиемы с последующей санацией и местным применением антисептических и ферментных препаратов. Во второй, гнойно-фибринозной, стадии необходимо разделение фибринозных сращений, удаление фибринозного налета с поверхности легкого и плевры, гнойно-некротических тканей из плевральной полости. Манипуляцию можно дополнять ультразвуковой кавитацией плевральной полости. При третьей стадии определяли оптимальные сроки проведения оперативного вмешательства либо традиционным открытым, либо видеоторакоскопическим способом. При тотальной и субтотальной эмпиеме плевры в гнойно-фибринозной стадии воспаления с деструкцией легкого произвести адекватную санацию под местным обезболиванием не всегда представлялось возможным. В таких ситуациях торакоскопию выполняли в последующие 1-2 сут под общим обезболиванием с раздельной вентиляцией легких.
Обязательным условием комплексного лечения эмпием плевры с деструкцией легочной ткани была санация полостей распада в легких. Использовали как неинвазивные (постуральный дренаж, ингаляции с муко-, бронхолитиками, дыхательная гимнастика в режиме положительного давления в конце выдоха), так и инвазивные методы (лечебно-санационные фибробронхоскопии, длительная трансбронхиальная катетеризация дренирующих бронхов и полостей деструкции в легких) [2, 7].
При эмпиеме плевры со стойкими бронхоплевральными свищами с целью ликвидации остаточной плевральной полости и создания условий для заживления свищей применяли временную эндобронхиальную окклюзию. Последнюю выполняли клапанными бронхоблокаторами, а при отсутствии таковых (трудности медицинского обеспечения) - поролоновыми обтураторами [9]. Дренирующий бронх, преимущественно сегментарный, определяли методом плеврохромобронхоскопии и на основании данных, полученных при видеоторакоскопии. При невозможности четко визуализировать дренирующий бронх использовали методику поисковой окклюзии. Временную окклюзию бронхов выполняли в ближайшие сутки после торакоскопической санации.
В ряде наблюдений с целью коррекции объема гемиторакса и создания условий для достижения плевродеза выполняли лечебный пневмоперитонеум либо путем повторных пункций брюшной полости, либо через установленный в брюшную полость катетер - метод «управляемого» пневмоперитонеума, что позволяло повторно инсуффлировать воздух в брюшную полость без повторных пункций.
Нами проведен сравнительный анализ лечения 162 больных с эмпиемой плевры (1-я группа), которым в лечебно-диагностический алгоритм была включена ранняя видеоторакоскопическая санация, с группой, состоящей из 110 больных (2-я группа), которым выполняли только дренирование плевральной полости. В 1-й группе отмечены более ранние сроки очищения и ликвидации остаточной плевральной полости (рис. 2). Рисунок 2. Эффективность ранней видеоторакоскопической санации. Количество исходов с полным выздоровлением увеличилось на 36,6%, причем у всех больных 1-й группы с первой стадией воспалительного процесса удалось добиться полного выздоровления. Частота перехода заболевания в хроническую форму снизилась на 18,2% (рис. 3). Рисунок 3. Исходы заболевания в группах больных с неспецифической эмпиемой плевры. Хронизация процесса чаще всего наблюдалась у больных с тяжелым фоновым и сопутствующими заболеваниями. Применение торакоскопической санации в ранние сроки позволило сократить необходимость проведения традиционных операций при наличии показаний, особенно при двусторонней локализации воспалительного процесса, когда показания к традиционным методам оперативного лечения ограничены. Сроки пребывания больных в стационаре сократились в среднем на 9 койко-дней.
Гангренозные поражения легких
Гангренозные поражения - наиболее тяжелые формы неспецифических легочных деструкций с традиционно высокой частотой неблагоприятных исходов, особенно при распространенных и осложненных процессах.
C 2003 по 2013 г. в отделении гнойной торакальной хирургии нашей больницы находились 79 больных с гангренозными поражениями легких, в том числе гангренозный абсцесс диагностирован у 39, распространенная гангрена доли, легкого - у 40. Эмпиема плевры как наиболее частое осложнение имела место более чем у 42 (53,2%) больных, причем при распространенной гангрене в 70% наблюдений. Общая летальность составила 22,7%.
Выбор метода лечения зависит не от формального обозначения процесса в легком (гангренозный абсцесс или гангрена), а от клинического проявления острого легочного нагноения и его течения [5]. Методы лечения гангренозных поражений можно разделить на следующие группы.
1. Симптоматическая терапия и малоинвазивная (бронхоскопическая) санация, закрытое дренирование плевральной полости при эмпиеме (пиопневмотораксе) у больных в исходно крайне тяжелом состоянии, обусловленном, как правило, поздней госпитализацией, когда оперативное лечение противопоказано. Эти больные умирают в течение 1-5 сут с момента поступления в стационар.
2. Дренирующие операции:
- трансторакальное (и/или трансбронхиальное) дренирование полости распада в легком. Закрытое дренирование как самостоятельный метод лечения должно применяться по следующим показаниям: при крайне тяжелом состоянии больных, которым оперативное лечение противопоказано; в качестве неотложной манипуляции для снятия интоксикации и предоперационной подготовки; при ограниченных неосложненных гангренозных поражениях небольшого объема;
- торакоскопическая некрсеквестрэктомия, санация и дренирование полости деструкции и плевральной полости.
3. Резекционные операции (пневмонэктомия, лобэктомия, резекции легкого в сочетании с плеврэктомией).
Перед хирургом зачастую стоит непростая задача в определении правильного подхода: раннее радикальное оперативное лечение или применение дренирующих операций. Тяжелое состояние больных, особенно при распространенной гангрене, осложненной эмпиемой плевры и воспалительным поражением противоположного легкого, ограничивает возможности ранних резекций. Крайне высокий риск развития вторичных бронхоплевральных и других осложнений при резекционных методах лечения расширяет показания к различным видам дренирующих операций: абсцессостомии, торакостомии. Методика торакоабсцессостомии с хорошими клиническими результатами используется в нашей практике с 1996 г. [3]. Показания к абсцессостомии: наличие свободных или формирующихся легочных секвестров; прогрессирующая деструкция легкого с выраженной интоксикацией; нарастание интоксикации при неэффективности других неоперативных методов лечения. Обязательными условиями выполнения абсцессостомии являются расположение полости деструкции в плащевой зоне и наличие спаечного процесса в зоне локализации полости распада. При наличии остаточной плевральной полости (пиопневмоторакс) прибегали к наложению торакостомы.
Показания к торакостомии: прогрессирующая деструкция легкого с эмпиемой плевры; гангренозные поражения с эмпиемой и обширным нагноением грудной стенки; распространенная эмпиема плевры с деструкцией легкого, свищами и выраженной гнойной интоксикацией; неэффективность других неоперативных методов лечения при условии выполнения их в полном объеме. Предпочтение отдавали методике наложения так называемой управляемой торакостомы, учитывая патогенез нарушения механизма дыхания, особенно при наличии бронхиального свища [6].

Эти виды открытого дренирования являются как этапными (перед радикальными резекционными вмешательствами), так и окончательными (без резекции легкого) методами с положительным результатом лечения и возможностью последующего выполнения торакопластики, торакомиопластики (рис. 4). Рисунок 4. Дренирующие операции как этапный и окончательный методы лечения. Дренирующие операции нами выполнены 36 больным (торакостомия - 20, абсцессостомия - 16) с достижением клинического эффекта у 31 больного и последующим закрытием абсцессоторакостом у 11 человек.
Видеоторакоскопическая некрсеквестрэктомия с санацией и дренированием полости распада и плевральной полости является операцией выбора при гангренозных поражениях легких как этапная дренирующая операция, так и окончательный метод лечения [4, 8]. Операцию выполняли под общим обезболиванием с однолегочной вентиляцией легких. Использовали два торакопорта. Применение монопортового режима допустимо только с диагностической целью и последующим дренированием. Способ выполнения торакоцентеза при неосложненных формах гангренозных поражений имел некоторые технические особенности. Введение торакопорта традиционным способом имеет высокий риск повреждения ткани легкого с развитием кровотечения. С целью безопасности торакоцентез выполняли путем большего (чем диаметр торакопорта) рассечения кожи, послойного расслоения мышц и рассечения париетальной и висцеральной плевры с помощью диатермокоагулятора. Место постановки второго порта определяли после осмотра полости, а установку порта осуществляли под визуальным контролем.
Проникнув в полость распада, оценивали характер и распространенность гнойно-деструктивного процесса в легком и плевре, выполняли разделение спаек, удаляли свободно лежащий легочный секвестр и гнойно-некротические ткани из плевральной полости, фибринозный налет с поверхности плевры и стенок полости распада. При наличии фиксированных участков некроза последние фрагментировали, частично удаляли с оставлением части секвестра в зоне расположения внутрилегочных сосудов из-за риска развития легочного кровотечения. Операцию заканчивали адекватным дренированием полости распада и эмпиемы. В последующем проводили санацию через дренаж с местным применением антисептических и ферментных препаратов и активной вакуум-аспирацией.
Этот метод оперативного пособия применен у 22 больных с положительным клиническим эффектом (в 7 наблюдениях достигнуто полное и клиническое выздоровление). Следует отметить, что абсцессостомия и торакоскопическая некрсеквестрэктомия должны рассматриваться не как взаимоисключающие, а как взаимодополняющие методы хирургического лечения, имеющие свои преимущества и недостатки.

Радикальные операции выполнены 7 больным (плевропневмонэктомия - 3, лобэктомия с плеврэктомией - 4) (см. таблицу). Исходы лечения с учетом отдаленных результатов были следующими: полное и клиническое выздоровление достигнуто у 51 (64,6%) больного, переход в хроническую форму отмечен в 10 (12,7%) наблюдениях, умерли 18 (22,7%) больных.
Таким образом, ранняя лечебно-диагностическая видеоторакоскопия является довольно эффективным хирургическим методом, позволяет улучшить непосредственные результаты лечения больных с эмпиемой плевры и сократить сроки пребывания в стационаре. Видеоторакоскопическая некрсеквестрэктомия служит альтернативной, малотравматичной и не менее эффективной операцией выбора и должна входить в лечебный алгоритм при гангренозных поражениях легких.
Эффективность операций при хронической эмпиеме плевры. Биопсия в торакальной хирургии
В данной работе рассматривается этиопатогенез, диагностика, особенности клинического течения и лечения эмпиемы плевры у 102 больных, пролеченных в отделении торакальной хирургии. По составу больных мужчин были больше, и они составили 77 %, а женщины 23 %. При изучении причины возникновения эмпиемы отмечен полиэтиологический характер начала болезни. По результатам проведенного исследования наиболее часто в 58 (56,8 %) случаях эмпиема плевры развивалась на фоне гнойно-воспалительных процессов в легких. У большинства больных в содержимом плевральной полости высеян стафилококк (29,1 %). Авторы считают, что применение традиционной рентгенографии, современных высокоинформативных методов лучевого и ультразвукового исследования, видеоторакоскопии, а также адекватное сочетание комплексной этиопатогенетической терапии, раннее дренирование плевральной полости и своевременное оперативное вмешательство занимает важное место в диагностике и лечении эмпиемы плевры.
3. Матвеев В.Ю., Хасанов Р.М., Галков Е.М., Фахрутдинов Р.Н., Ибрагимов А.И. Комбинированное хирургическое лечение эмпиемы плевры с применением видеоторакоскопии // Практическая медицина. – 2012. – № 8, т. 2. – С. 111–116.
4. Порханов В.А. Торакоскопическая и видеоконтролируемая хирургия легких, плевры и средостения: дис. докт. Мед. – М., 1996. – 233 с.
5. Цеймах Е.А., Левин А.В., Зимонин П.Е., Самуйленков А.М. Частота возникновения, эмпиемы плевры пункционная терапия, закрытое дренирование плевральной полости. Часть I // Туберкулез и болезни легких. – 2009. – № 8. – С. 3–9.
6. Цеймах Е.А. Лечение острых эмпием плевры и пиопневмоторакса // груд. и сердечно-сосуд. хир. – 1999. – № 1. – С. 51–54.
7. Ясногородский О.О., Шулутко А.М., Панюшкин П.В. Возможности малоинвазивной техники в лечении неспецифической эмпиемы плевры // росс. мед. журнал. – 2004. – № 3. – С. 32–36.
8. Simmers T.A., Jie C., Sie B. Paraneumonic effusions // Thorac. Cardiovasc. Surg. – 2009. – vol. 47, № 2. – Р. 77–81.
9. Hollaus P.H., Lax F., Wurnig P.N. Guided percutaneous drainage for empiema // Eur. J. Cardiovasc. Surg. – 2009. – vol. 16, № 3. – Р. 283–286.
Диагностика и лечение эмпиемы плевры остается актуальной проблемой в хирургии. Под термином «эмпиема плевры» или «пиоторакс» принято считать ограниченное или распространенное воспаление висцеральной и париетальной плевры, протекающее с накоплением гноя в плевральной полости и сопровождающееся признаками гнойной интоксикации [1]. По данным ряда авторов почти у 90 % больных эмпиема плевры возникает в результате осложнений гнойно- воспалительного процесса в легких (на фоне острой пневмонии 4 %, абсцесса легкого – 9–11 %, при гангрене легкого – 80–95 %) [2, 3]. Как следствие ранений и травм органов грудной клетки – 6–12 %, основной причиной при этом является неликвидированный посттравматический плеврит и гемоторакс [1 ,4, 5]. Послеоперационные эмпиемы плевры составляют в структуре причины от 2 до 28 %, наиболее часто возникают после пневмонэктомии [5, 8]. При бактериологическом исследовании содержимого плевральной полости грамотрицательная флора встречается в 20–30 % случаев. Грамположительная флора высеивается в 30–40 %, преимущественно S. aureus, S. pneumoniae, S. pyogenes. В 20–30 % флора является смешанной, в сочетании с неклостридиальными анаэробами [5–7].
Цель исследования – изучение основных причин и факторов приводящих к гнойному воспалению плевры, выработки тактических и технических решений, направленных на улучшение результатов комплексного лечения эмпиемы плевры с использованием современных технологий.
Материалы и методы исследования
Под наблюдением находились 102 больных с эмпиемой плевры, в возрасте от 17 до 80 лет, из них 79 (78 %) мужчин и 2 (22 %) женщин (табл. 1). Из числа поступивших сельскими жителями были 89 (88 %) больных, и городских жителей было 12 (11 %). Из 102 пролеченных больных у 60 (59 %) была хроническая форма, а у 42(41 %) острая форма эмпиемы плевры. Сплошное поражение плевры гнойно-воспалительным процессом наблюдалось у 76 (75 %) больных, а у 26 (25 %) была ограниченная (осумкованная) форма болезни. Правосторонней эмпиемой страдали 65 (64 %) больные, левосторонней 37 (36 %).
Распределение больных по возрасту и полу (n – 102)
из них в возрасте (в годах)
Рис. 1. Динамика роста эмпиемы плевры по годам
Клинические обследования проводились по общепринятой схеме. Учитывали данные анамнеза, жалобы больного, проводились объективные и дополнительные специальные методы обследования. С целью диагностики применены традиционная R-графия, компьютерная томография (КТ), ультразвуковое исследование (УЗИ) органов грудной клетки, торакоскопия плевральной полости, лабораторно-микробиологические исследования содержимого плевральной полости и гистология биопсийного материала из плевры.
Результаты исследования и их обсуждение
Результаты исследования показали, что в динамике отмечается рост числа больных с эмпиемой плевры (рис. 1), с 8 случаев в 2010 г. до 26 в 2016 г.
Последние годы часто поступают больные в тяжелом состоянии с распространённой формой болезни, особенно после прорыва нагноившейся эхинококковой кисты, кистозных полостей и абсцесса легких в плевральную полость. Среди наших больных в зависимости от локализации жидкостных образований в плевральной полости нами установлены следующие виды эмпиемы плевры (рис. 2).
При изучении причины возникновения эмпиемы по результатам нашего исследования (табл. 2) у 45 больных, то есть 53,8 % случаях, эмпиема плевры развилась при пневмониях осложненных в виде и плевритов различного происхождения в результате проникновения инфекции в плевральную полость лимфогенным или гематогенным путями. Из них в 21 случаях нагноения плеврального выпота сопровождались появлением очагов распада в легочной паренхиме с образованием бронхоплеврального свища. В 15 (11,5 %) случаях поступили больные с прорывом нагноившейся эхинококковой кисты в плевральную полость с формированием пиопневмоторакса. У 13 (12,7 %) больных в результате прорыва в плевральную полость одного или нескольких субплеврально расположенных абсцессов, гнойных кист при поликистозах легкого развился пиопневмоторакс.
Причины проводящие к эмпиеме плевры распространённого и осумкованного характера с формированием бронхоплеврального свища. В 8 (7,8 %) случаях с переломами ребер в результате нагноения гемоторакса наступила эмпиема плевры. У 8 (7,8 %) пациентов причиной эмпиемы был несвоевременно установленный разрыв воздушных кист легкого. У 6 (5,8 %) больных сахарным диабетом на фоне диабетической нефропатии гидроторакс осложнился эмпиемой плевры. После оперативного вмешательства на органах грудной клетки и брюшной полости в 5 (4,9 %) случаях впоследствии инфицирования плевральной полости организовалась эмпиема плевры. У 2 (1,9 %) больных в результате распада новообразования в легком развилась эмпиема плевры. Наличие бронхоплеврального свища в наших наблюдениях всегда явилось поддерживающим и усугубляющим фактором гнойно-воспалительного процесса в плевральной полости, придавая течению эмпиемы плевры торпидный характер.
Рис. 2. Виды эмпием плевры (схема): 1 – верхушечная; 2 – междолевая; 3 – базальная; 4 – пристеночная; 5 – пиопневмоторакс; 6 – прорыв гноя под кожу
В зависимости от начала болезни и продолжительности воспалительного процесса больных разделили на 2 группы. В первую группу с острой эмпиемой плевры вошел 41 больной, у которых с начала болезни прошло 8–12 недель. Во вторую группу с хроническим течением болезни включен 61 больной, когда с начало заболевания у них протекало более 12 недель. Хронизацию острого процесса обусловливали разнообразные факторы. Чаще к хронической эмпиеме приводило неэффективное лечение острых легочных нагноений, осложнившихся пиопневмотораксом.
В нашем наблюдении клинические проявления эмпиемы плевры независимо от причины возникновения в большинстве случаев имели общие симптомы. В основном больных беспокоили следующие жалобы: кашель с выделением гнойной мокроты, одышка, боли в груди, усиливающиеся при дыхании, повышение температуры тела, а также признаки интоксикации организма. Длительные и частые приступы кашля с отделением значительного количества мокроты свидетельствовали о наличии бронхоплеврального свища. В начальных стадиях болезни больные с тотальной и субтотальной эмпиемой из-за резкой боли и одышки часто принимали вынужденное полусидящее положение. При отграниченных (осумкованных) и малых эмпиемах болевой синдром был выражен слабее.
При исследовании грудной клетки отмечали отставание пораженной половины при дыхании. Межреберные промежутки были расширены и сглажены вследствие давления экссудата. Для скопления экссудата в плевральной полости характерно было ослабление или отсутствие голосового дрожания и дыхательных шумов. У больных, когда содержимым плевральной полости оказался только экссудат, верхняя граница тупости соответствовала линии Эллиса – Дамуазо – Соколова (линия, проходящая от позвоночника латерально и вверх до задней подмышечной линии, затем вниз и кпереди до среднеключичной линии). Наиболее часто при скоплении большого количества гноя в плевральной полости у больных наблюдалось смещение органов средостения в здоровую сторону и сдавление здорового легкого. У больных пиопневмотораксом выявляли тупой перкуторный звук под участком с верхней горизонтальной границей, соответствующей скоплению гноя, и тимпанический звук над участком скопления воздуха. Аускультативно определяли ослабление или почти полное отсутствие дыхательных шумов и усиленную бронхофонию в зоне скопления экссудата. При наличии бронхоплеврального свища и хорошо дренируемой через бронх полости отмечали усиленное бронхиальное дыхание (амфорическое). При этом у больных появлялась обильная гнойная мокрота с неприятным запахом. В 25 случаях у наших больных наблюдали клинику полиорганной недостаточности.
Со стороны анализов изменения в общеклинических показателях крови и мочи при эмпиеме плевры были такие же, как и при других тяжелых гнойных процессах. В общем анализе крови отмечали высокий лейкоцитоз (выше 10×10 9 /л), резкий сдвиг лейкоцитарной формулы влево, увеличение СОЭ. Нередко наблюдали анемию. Содержание белка в плазме уменьшалось, главным образом за счет альбумина. В моче обнаруживали альбуминурию, наличие зернистых и гиалиновых цилиндров
В диагностике и определении показании к подбору антибиотиков важное место занимало цитологическое и гистологическое исследование содержимого плевральной полости.
Причины возникновения эмпиемы
После пневмонии и плеврита
Прорыв эхинококковой кисты в плевральную полость
Осложнение гнойно-некротических процессов в легких (абсцесс, поликистоз)
Буллезная болезнь легких осложненная пиопневмотораксом
После травмы (гемоторакс)
После хирургического вмешательства на органах грудной и брюшной полостей
Высеянные флоры при бакпосеве содержимого плевральной полости
Как указано на табл. 3, при бактериологическом исследовании из содержимого плевральной полости высеяно staphylococci у 30 (29,4 %) больных, в 18 (17,6 %) случаях pneumococci, а klebsiella pneumonia у 15 (14,7 %) пациентов. У 15 (14,7 %) больных обнаружено streptococci, а hemofilus influenza было в 14 (13,7 %) случаях, candida alvicans выделен из пунктата у 10 (9,9 %) больных.
В нашей практике важнейшую роль в диагностике эмпиемы плевры играло рентгенологическое исследование. Всем больным в процессе диагностики и лечения неоднократно произведена рентгенография органов грудной клетки в 2 проекциях. Посредством этого метода получили представление о локализации, распространенности и количественной характеристике процесса в полости плевры.
В настоящее время с появлением современных методов лучевой диагностики при сложных ситуациях удаётся установить точный, достоверный диагноз. В нашей практике у 20 больных в сложных случаях заключительный диагноз установлен с применением рентгено-компьютерной томографии (РКТ). Применение РКТ позволяло детально оценить осумкованные выпоты, утолщение плевральных листков, очаговые образования в плевре.
Важное место в диагностике занимает метод ультразвукового исследования плевральной полости. С помощью УЗИ у 39 больных, при ограниченных жидкостных образованиях, удалось определять локализации и дренировать осумкованные плевральные полости. Из них в 6 случаях установлено наличие эхинококковой кисты в нижних отделах легких с прорывам в плевральную полость.
Последнее время начали внедрять видеоторакоскопию. С использованием видеоторакоскопа в 17 случаях проводили визуальный осмотр полости плевры, поверхность легкого, определяли характер жидкости и брали биопсию для гистологического исследования.
В нашей практике лечение больных с эмпиемой плевры сводилось в первую очередь к воздействию на основное заболевание, с учетом его формы и фазы, патогенеза плевральной экссудации и характера выпота, а также общего состояния больных. Как наш опыт работы показывает, важнейшим требованием позволяющим добиться наибольшего эффекта при эмпиемах плевры, любого происхождения, является раннее и длительное проведение комплекса различных консервативных мероприятий и хирургических вмешательств. Основными звеньями комплексной патогенетической терапии больных мы считаем следующие положения:
а) применение антибиотиков для подавления, уменьшения или ослабления антигенных влияний, исходящих из зоны основного процесса и вызывающих воспалительную реакцию плевры;
б) санации плевральной полости путем эвакуации содержимого, а при необходимости и промываний;
в) применение десенсибилизирующих и противовоспалительных средств, направленных на борьбу с повышенной проницаемостью плевры и для воздействия на местные и общие проявления самого плеврита.
У подавляющего большинства больных лечение эмпиемы начали с плевральной пункции. При получении гноя мы всегда дренировали плевральную полость. Дренирование было активным (при использовании устройств для создания отрицательного давления 10–30 см вод. ст.) или пассивным (например, по Бюллау). В 56 случаях гнойно-воспалительный процесс в плевре разрешился в результате адекватного дренирования и регулярного промывания антисептиками плевральной полости, а также комплексной консервативной терапии. Для промывания применяли раствор фурациллина 1:1000, 0,2 % декосона, водный раствор хлоргексидина.
При хронической эмпиеме плевры независимо от причин возникновения болезни, часто требовалось хирургическое вмешательство. Хирургическое лечение всегда было и в настоящее время остается трудной задачей. Длительный гнойно-воспалительный процесс, наличие бронхо-плеврального свища часто привадило к грубым изменениям со стороны париетальной и висцеральной плевры, сформированию осумкованных полостей. В нашей практике многие годы торакопластика была наиболее эффективным хирургическим вмешательством при хронической эмпиеме плевры, хотя она отличалась травматичностью и приводила к тяжелой деформации грудной клетки. Последние десятилетия торакопластику применяем очень редко, так как она почти изжила себя из-за нефизиологичности и недостаточной эффективности. Мы часто стали проводить радикальные операции – плеврэктомия (операция Делорма). В 21 случаях произведена данная операция с удовлетворительным результатом. При этой операции полностью удаляется вся измененная париетальная, а также и висцеральная плевра (иногда это удается сделать единым блоком, одним «мешком»). А у 10 пациентов с кистозным поражением легкого операция завершилась лобэкотомией и частичной декортикацией легкого. При наличии бронхиального свища производили резекцию легочной ткани и несущий свищ или ушивали свищ одним из многочисленных способов. При достижении герметизации легкое хорошо расправляется, заполняет плевральную полость, что позволяет восстановить его функцию и ликвидировать гнойную полость. У 15 больных при прорыве в плевральную полость нагноившейся эхинококковой кисты легкого и диафрагмальной поверхности печени удалена свободно находящаяся хитиновая оболочка, а также произведена санация и частичная декортикация легкого. Операция плеврэктомия сложна и травматична. Она иногда осложнялась тяжелым кровотечением, травматическим шоком, поэтому проводилась тщательная предоперационная подготовка больного, целью которой было – уменьшить анемию, гипопротеинемию, улучшить функцию дыхания.
В послеоперационном периоде наблюдали различные осложнения: кровотечения в плевральную полость у 3 больных, рецидив бронхиального свища и эмпиемы плевры в 8 случаях. При кровотечениях во всех случаях произведена реторакотомия и кровотечение остановлено. В основном источником кровотечений оказались мелкие сосуды по всей поверхности удаленной плевры. При рецидиве болезни в 2 случаях произведена повторная операция, в 6 случаях мы достигли положительного результата консервативным путем. Все операции проводились общим наркозом с использованиям эндобронхиальной двухпросветной трубки для раздельной интубации легких.
Заключение
Таким образом, при анализе пролеченных случаев в динамике отмечается рост числа больных с эмпиемой плевры, с 8 случаев в 2010 г. до 26 в 2016 г. Применение компьютерной томографии, УЗИ и видеоторакоскопии существенно улучшило диагностику эмпиемы плевры, особенно при осумкованных формах. При адекватном сочетании комплексной этиопатогенетической терапии, раннего дренирования плевральной полости и своевременного радикального оперативного вмешательства, заметно улучшились результаты лечения при острых и хронических формах эмпиемы плевры. Уменьшились случаи рецидива болезни, а также значительно сократились сроки пребывания больного в стационаре от 24,5 койко-дней в период до 2010 года, до 17,8 дней за 2010–2016 годы. Лечение эмпиемы плевры как полиэтиологического заболевания должно быть комплексным.
Читайте также:
