Перикардит при инфаркте миокарда. Синдром Дресслера.
Обновлено: 25.04.2024
Синдром Дресслера (постинфарктный синдром) — сочетание перикардита с плевритом, реже пневмонией и эозинофилией, развивающееся на 3–4-й неделе с момента возникновения ИМ; обусловлено сенсибилизацией организма к деструктивно измененным белкам миокарда. Выделяют также посткардиотомный (постперикардиотомический) синдром, являющийся частным случаем раннего синдрома Дресслера и возникающий в ближайшем периоде после операций, сопровождающихся вскрытием полости перикарда. Статистические данные. Синдром Дресслера наблюдают у 1–3% больных ИМ и после 35–50% перикардиотомий.
Патогенез. Существенное значение имеют аутоиммунные реакции.
Клинические проявления • Синдром Дресслера характеризуется болью в грудной клетке, лихорадкой, полисерозитом и склонностью к рецидивированию. Классической триадой постинфарктного синдрома считают перикардит, плеврит, пневмонит • Развивается постинфарктный синдром через 2–11 нед от начала ИМ (чаще без зубца Q) с появления боли в грудной клетке. Затем присоединяется лихорадка до 38–40 °С. В дальнейшем возникают гидроперикард и гидроторакс • Продолжительность постинфарктного синдрома от 3 сут до 3 нед.
Диагностика. Помогают рентгенологические и ЭхоКГ-методы исследования.
Лечение • Постперикардиотомный синдром Дресслера — назначение НПВС. Применение ГК не улучшает результатов лечения, но замедляет течение раневого процесса • При постинфарктном синдроме Дресслера, толерантном к лечению НПВС, допустимо назначение ГК в средних дозах коротким курсом. Прямые антикоагулянты, если нет абсолютной необходимости в их назначении, желательно отменить.
МКБ-10 • I24.1 Синдром Дресслера
Код вставки на сайт
Синдром Дресслера
Синдром Дресслера (постинфарктный синдром) — сочетание перикардита с плевритом, реже пневмонией и эозинофилией, развивающееся на 3–4-й неделе с момента возникновения ИМ; обусловлено сенсибилизацией организма к деструктивно измененным белкам миокарда. Выделяют также посткардиотомный (постперикардиотомический) синдром, являющийся частным случаем раннего синдрома Дресслера и возникающий в ближайшем периоде после операций, сопровождающихся вскрытием полости перикарда. Статистические данные. Синдром Дресслера наблюдают у 1–3% больных ИМ и после 35–50% перикардиотомий.
Патогенез. Существенное значение имеют аутоиммунные реакции.
Клинические проявления • Синдром Дресслера характеризуется болью в грудной клетке, лихорадкой, полисерозитом и склонностью к рецидивированию. Классической триадой постинфарктного синдрома считают перикардит, плеврит, пневмонит • Развивается постинфарктный синдром через 2–11 нед от начала ИМ (чаще без зубца Q) с появления боли в грудной клетке. Затем присоединяется лихорадка до 38–40 °С. В дальнейшем возникают гидроперикард и гидроторакс • Продолжительность постинфарктного синдрома от 3 сут до 3 нед.
Диагностика. Помогают рентгенологические и ЭхоКГ-методы исследования.
Лечение • Постперикардиотомный синдром Дресслера — назначение НПВС. Применение ГК не улучшает результатов лечения, но замедляет течение раневого процесса • При постинфарктном синдроме Дресслера, толерантном к лечению НПВС, допустимо назначение ГК в средних дозах коротким курсом. Прямые антикоагулянты, если нет абсолютной необходимости в их назначении, желательно отменить.
Синдром Дресслера

Постинфарктный синдром (или синдром Дресслера) — реактивное аутоиммунное осложнение инфаркта миокарда, развивающееся через 2—6 недель после его начала.
Частота развития
Первоначально считалось, что синдром Дресслера возникает примерно у 4% больных, перенесших инфаркт миокарда. C учетом атипичных и малосимптомных форм частота его развития значительно выше – 15–23 %, а по некоторым источникам достигает 30 %. Однако в последние годы частота синдрома Дресслера уменьшилась. Причинами могут быть широкое использование нестероидных противовоспалительных средств (ацетилсалициловой кислоты) и распространение реперфузионных методов лечения ИМ, уменьшающих объем повреждения мышцы сердца. Другой причиной снижения частоты развития синдрома Дресслера может быть включение в комплекс терапии инфаркт миокарда ингибиторов ангиотензинпревращающего фермента, антагонистов альдостерона и статинов, вследствие их иммуномодулирующего и противовоспалительного действия. Постинфарктый синдром развивается в подостром периоде (не ранее 10-го дня от момента заболевания) у 3—4 % пациентов, перенёсших инфаркт миокарда.
Причины развития
Основная причина синдрома Дресслера – инфаркт миокарда. Считается, что синдром Дресслера чаще развивается после крупноочаговых и осложненных инфарктов, а также после кровотечений в полость перикарда. Синдром Дресслера, точнее синдром постповреждения сердца, может развиваться после кардиохирургических вмешательств (постперикардиотомический синдром, посткомиссуротомический синдром). Помимо этого, типичные признаки синдрома Дресслера могут появляться после других повреждений сердца (ранение, контузия, непроникающий удар в область грудной клетки, катетерная абляция). В настоящее время синдром Дресслера рассматривается как аутоиммунный процесс, обусловленный аутосенсибилизацией к миокардиальным и перикардиальным антигенам. Определенное значение придается также антигенным свойствам крови, попавшей в полость перикарда.
При постинфарктном синдроме наблюдаются изменения и в клеточном иммунитете. Так, имеются данные, что при синдроме Дресслера значительно повышен уровень цитотоксических T-клеток. Этиологическим фактором синдрома Дресслера может быть инфекция, в частности вирусная, поскольку у больных, у которых этот синдром развился после кардиохирургических вмешательств, часто регистрируют повышение титра противовирусных антител.
Симптомы и течение
Развивается на 2–4-й неделе инфаркта миокарда, однако эти сроки могут уменьшаться – «ранний синдром Дресслера» и увеличиваться до нескольких месяцев, «поздний синдром Дресслера». Иногда течение синдрома Дресслера принимает агрессивный и затяжной характер, он может длиться месяцы и годы, протекать с ремиссиями и обострениями. Основные клинические проявления синдрома: лихорадка, перикардит, плеврит, пневмонит и поражение суставов. Лихорадка при синдроме Дресслера не имеет какой-либо строгой закономерности. Как правило, она бывает субфебрильной, хотя в отдельных случаях может быть фебрильной или вообще отсутствовать.
Перикардит является обязательным элементом синдрома Дресслера. Клинически он проявляется болью в перикардиальной зоне, которая может иррадиировать в шею, плечо, спину, брюшную полость. Боль может быть острой приступообразной (плевритическая) или давящей, сжимающей (ишемической). Она может усиливаться при дыхании, кашле, глотании и ослабевать в вертикальном положении или лежа на животе. Она длительная и исчезает или ослабевает после появления в полости перикарда воспалительного экссудата. Главный аускультативный признак перикардита – шум трения перикарда: в первый день болезни при внимательной аускультации он определяется у абсолютного большинства (до 85 %) больных. Шум лучше всего выслушивается у левого края грудины, при задержке дыхания и наклоне туловища пациента вперед. В классическом варианте он состоит из трех компонентов – предсердного (определяется в систолу) и желудочкового (систолического и диастолического). Как и боль, шум трения перикарда уменьшается или исчезает вовсе после появления в полости перикарда выпота, раздвигающего трущиеся листки перикарда. Обычно перикардит протекает нетяжело: уже через несколько дней боли стихают, а экссудат в полости перикарда почти никогда не накапливается в таком количестве, чтобы ухудшить кровообращение, хотя иногда могут появиться признаки тяжелой тампонады сердца. Иногда воспалительный процесс в перикарде при синдроме Дресслера принимает затяжной рецидивирующий характер и заканчивается развитием констриктивного перикардита. При применении антикоагулянтов на фоне синдрома Дресслера возможно также развитие геморрагического перикардита, хотя подобное осложнение может быть и при отсутствии антикоагулянтной терапии.
Плеврит. Проявляется болью в боковых отделах грудной клетки, усиливающейся при дыхании, затруднением дыхания, шумом трения плевры, притуплением перкуторного звука. Он может быть сухим и экссудативным, односторонним и двусторонним. Нередко плеврит носит междолевой характер и не сопровождается типичными физикальными симптомами.
Пневмонит. Пневмонит при синдроме Дресслера выявляется реже, чем перикардит и плеврит. Если очаг воспаления достаточно велик, также отмечается притупление перкуторного звука, ослабленное или жесткое дыхание, появление фокуса мелкопузырчатых хрипов. Возможен кашель и выделение мокроты, иногда с примесью крови, что всегда вызывает определенные диагностические трудности.
Поражение суставов. Для синдрома Дресслера характерно появление так называемого «синдрома плеча»: болезненных ощущений в области плечелопаточных суставов, чаще слева, ограничение подвижности этих суставов. Вовлечение в процесс синовиальных оболочек нередко приводит к возникновению болей и в крупных суставах конечностей.
Другие проявления. Проявлением постинфарктного синдрома может быть сердечная недостаточность вследствие диастолической дисфункции, геморрагический васкулит и острый гломерулонефрит.
Методы исследования
Лабораторные данные. Часто отмечается повышение СОЭ и лейкоцитоз, а также эозинофилия. Весьма характерно резкое повышение уровня С-реактивного белка. У больных с синдромом Дресслера регистрируются нормальные уровни маркеров повреждения миокарда (МВ-фракция креатинфосфокиназы (МВ-КФК), миоглобин, тропонины), хотя иногда отмечается их незначительное повышение, что требует проведения дифференциальной диагностики с рецидивом инфаркта миокарда.
Электрокардиография (ЭКГ). При наличии перикардита на ЭКГ определяются диффузный подъем сегмента ST и, периодически, депрессия сегмента PR, за исключением отведения aVR, в котором наблюдаются депрессия ST и подъем PR. По мере накопления экссудата в полости перикарда может снизиться амплитуда комплекса QRS.
Эхокардиография. При накоплении жидкости в полости перикарда выявляется сепарация его листков и могут появиться признаки тампонады сердца. Для синдрома Дресслера не характерен большой объем жидкости в полости перикарда – как правило, сепарация листков перикарда не достигает 10 мм в диастолу.
Рентгенография. Обнаруживают скопление жидкости в плевральной полости, междолевой плеврит, расширение границ сердечной тени, очаговые тени в легких.
Компьютерная или магнитнорезонансная томография также выявляют жидкость в полости плевры или перикарда и легочную инфильтрацию.
Плевральная и перикардиальная пункция. Извлеченный из полости плевры или перикарда экссудат может быть серозным или серозно-геморрагическим. При лабораторном исследовании в нем определяется эозинофилия, лейкоцитоз и высокий уровень С-реактивного белка.
Лечение
Нестероидные противовоспалительные препараты (НПВС). Препаратом выбора при синдроме Дресслера традиционно считается ибупрофен (400– 800 мг/сут). Реже используют аспирин. Хирургическое лечение применяется при констриктивном перикардите.
Осложнения
Тампонада сердца, геморрагический или констриктивный перикардит, окклюзия (сдавление) коронарного шунта и редко – анемия.
Прогноз
Прогноз при синдроме Дресслера, как правило, благоприятный. Вместе с тем его течение иногда принимает затяжной рецидивирующий характер. Кроме того, имеются данные о том, что выживаемость в течение 5 лет среди перенесших этот синдром, хотя и незначительно, но снижается.
Аутоиммунный процесс развивающийся после инфаркта миокарда и проявляющийся перикардитом, плевритом, воспалительными заболеваниями суставов и сосудов. Лечение проводится с помощью противовоспалительных препаратов.
Синдром Дресслера (постинфарктный синдром)
Опасность инфаркта миокарда состоит не только в том, что он приводит к нарушению функционирования сердечно-сосудистой системы. После этого заболевания развиваются различные осложнения, которые способны намного ухудшить качество жизни. Одно из таких осложнений – синдром Дресслера, или постинфарктный синдром.
Каждому пациенту, обратившемуся к нам, мы готовы предложить плановую и экстренную помощь при сердечно-сосудистых заболеваниях. Для лечения пациентов с синдромом Дресслера врачи-кардиологи ОН КЛИНИК применяют самые современные и действенные методы, одобренные в лучших клиниках Европы и Израиля.
Поскольку все большее количество пациентов страдает сердечно-сосудистыми заболеваниями и нуждается в помощи высококвалифицированных специалистов, кардиология является одним из самых востребованных и стремительно развивающихся направлений в нашей клинике. Мы стремимся идти в ногу со временем и предлагаем пациентам лучшее из имеющегося в мировой медицине. Если Вас беспокоит сердце – не ждите осложнений, звоните и записывайтесь к нам на прием!
Что такое синдром дресслера?
Впервые это заболевание было описано немецким ученым Вильямом Дресслером в средине XX века и названо его именем. Постинфарктный синдром является аутоиммунной патологией, которая дает о себе знать такими заболеваниями, как перикардит, плеврит, пневмонит, воспалительные заболевания суставов. Атипичная форма синдрома Дресслера может привести к появлению проблем в функционировании легких, почек и желудочно-кишечного тракта.
По течению и периоду развития синдром Дресслера разделяют на ранний, который возникает сразу же после инфаркта миокарда, и поздний, развивающийся через несколько недель и даже месяцев. Согласно статистике, постинфарктный синдром развивается примерно у 4% пациентов, перенесших инфаркт миокарда. Однако, по мнению врачей, с этим осложнением сталкивается намного больше пациентов, так как синдром Дресслера может протекать малосимптомно и атипично, что затрудняет диагностику.
Симптомы синдрома дресслера
Среди самых распространенных симптомов постинфарктного синдрома:
- сжимающие или острые боли в груди;
- иррадиация болей в плечи, руки, ощущение онемения кожи;
- сильная одышка, сухой кашель с прожилками крови;
- ощущение давления в грудной клетке;
- повышенная температура тела, сильная потливость;
- кожная сыпь;
- боли в суставах;
- общее недомогание и плохое самочувствие.
Наличие любого из этих симптомов должно послужить поводом для немедленного обращения к врачу. Если Вы или Ваш близкий человек недавно пережили инфаркт и имеются жалобы на дискомфорт в области сердца – не медлите, записывайтесь на прием к кардиологу! В экстренных случаях у нас в медцентре врачи готовы принять пациента без записи.
ОН КЛИНИК – это современная диагностика и эффективное лечение кардиологических заболеваний. Обращайтесь, преодолеем болезнь вместе!

Соколова С.В., терапевт. Кардиология в ОН КЛИНИК: как снизить риск наступления инфаркта.
Диагностика и лечение синдрома дресслера в ОН КЛИНИК
В Международном медицинском центре ОН КЛИНИК работают лучшие кардиологи, которые постоянно повышают квалификацию в нашей стране и за рубежом. В нашей клинике применяются только оригинальные препараты и оборудование наиболее известных мировых производителей, качество которых подтверждено сертификатами соответствия.
Особое внимание у нас в клинике уделяют диагностике, ведь если заболевание протекает бессимптомно или с неявными симптомами, как это случается с синдромом Дресслера, обнаружить его можно только при помощи тщательного обследования и применения высокоточных современных аппаратов.
Диагностика при подозрении на синдром Дресслера включает в себя анализ анамнеза заболевания, жалоб пациента, физикальный осмотр врача и следующие виды исследований:
- электрокардиограмма;
- эхокардиография;
- рентгенография грудной полости;
- магнитно-резонансная томография;
- компьютерная томография;
- общие анализы мочи и крови, биохимический анализ крови.
Лечение постинфарктного синдрома медикаментозное и заключается в приеме кардиотропных, гиполипидемических и нестероидных противовоспалительных препаратов. Также могут потребоваться глюкокортикостероиды, бета-блокаторы, антикоагулянты и анальгетики для снятия выраженного болевого синдрома. Иногда требуется госпитализация. Все препараты пациенту должен подбирать врач-кардиолог, самолечение недопустимо и может привести к непоправимым последствиям!
Если у Вас или Ваших близких синдром Дресслера, подозрение на это заболевание или общее плохое самочувствие и постинфарктные перебои в работе сердца – приезжайте в ОН КЛИНИК, где Вашим здоровьем займутся профессионалы в области кардиологии.
Неотложная кардиология. Часть 2. Разрыв сердца, аневризмы, синдром Дресслера.
Сегодня поговорим о разрывах сердца, о перикардитах, о синдроме Дресслера, о ранней постинфарктной стенокардии, об аневризмах сердца, а также рассмотрим осложнения со стороны ЖКТ и почек при инфаркте миокарда.
Эта статья в формате видеолекции здесь.
Разрывы сердца делятся на внешние и внутренние. Внешние могут быть мгновенные либо с формированием ложной аневризмы, когда это происходит постепенно, например, при физической нагрузке. В месте разрыва формируется тромб, так называемая ложная аневризма. Поскольку соединительной ткани в этом месте не сформировалось, то далее при очередной физической нагрузке этот разрыв будет глубже.
Внутренние разрывы чаще всего связаны с разрывом межжелудочковой перегородки при передней локализации инфаркта миокарда или разрыва сосочковых мышц при задней локализации инфаркта миокарда.
Диагностика: ЭХОКГ, вентрикулография
Лечение: хирургическое

Так выглядит гемотампонада при внутреннем разрыве (секционный снимок), когда сформировался тромб, который прикрывал разрыв.

На этой фотографии кружком обведен надрыв сосочковой мышцы.
Аневризма сердца
Аневризма сердца – это истонченный участок миокарда, утративший способность сокращаться. Фактически любой некротизированный участок, который утратил способность сокращаться, можно назвать аневризмой. Но в клиническом плане про аневризму говорят, когда она влияет на гемодинамику.
При инфарктах миокарда в 80% случаев формируется аневризма. Чем больше площадь инфаркта, тем больше вероятность развития аневризматического повреждения. Кроме того, вероятность развития аневризмы увеличивается при нарушении режима.
Аневризмы могут быть плоские и мешотчатые. Если аневризма плоская (диффузная), она может не влиять на гемодинамику. Мешотчатая аневризма способствует формированию тромботической массы, ухудшает гемодинамику и повышает опасность тромботических осложнений.
Диагностика: осмотр, аускультация, ЭКГ, радионуклидная сцинтиграфия, вентрикулография.
Перикардит
Перикардиты после инфарктов нередкое состояние. Перикардит при инфаркте называется перикардитом Кернига. Это реактивный перикардит, связанный с аутоиммунными механизмами. Возникает воспалительная реакция перикарда в ответ на частицы некроза, которые вымываются в кровь при инфаркте и вызывают аутоиммунную реакцию воспаления. Развивается, как правило, в первые дни после инфаркта. Когда появляется выпот в полости перикарда – это является показанием для прекращения введения гепарина. Обращаем внимание, что тема заболеваний сердца, в том числе и перикардитов, также подробно разбирается на наших курсах повышения квалификации по терапии и общей врачебной практике.
Болевой синдром может быть не выражен (боли в левой половине грудной клетки, тупые, ноющие, длительные), летучий шум трения перикарда. Могут быть нарушения ритма. Пациенту сложно лежать на спине, удобнее на животе либо пациент сидит на кровати, ставит ноги на табуретку.
ЭКГ в данном случае будет характерно для инфаркта, а не для перикардита. Если перикардит Кернига случается на фоне инфаркта, то преобладать на ЭКГ будут инфарктные изменения.
Диагностика: ЭХОКГ
Лечение: НПВС, ГКС (преднизолон 20-30 мг/сут 6 дней). Пункция при геморрагическом выпоте.
Представлен гнойный перикардит. В полости перикарда виден гнойный экссудат.
Реактивный перикардит Кернига может быть изолированным, самостоятельным осложнением. А может быть в рамках синдрома Дресслера.
Синдром Дресслера
При синдроме Дресслера перикардит сочетается с плевритом, пневмонитом и поражением суставов и носит аутоиммунный характер. В рамках этого синдрома клиника перикардита является ведущей. В суставах поражаются синовиальные оболочки.
Различают ранний Дресслер, который развивается на первой неделе после инфаркта миокарда и поздний Дресслер, который может сформироваться через несколько месяцев после случившегося инфаркта миокарда.
Механизмы развития синдрома Дресслера - аутоиммунный и вирусный.
Пациент жалуется на кардиалгии, повышение температуры, боли в суставах.
Можно выслушать шум трения плевры и мелкопузырчатые хрипы.
В крови может быть лейкоцитоз, повышение СОЭ. Выпот может быть серозный или геморрагический.
Плеврит может быть сухим или экссудативным. Если нет шума трения плевры, тогда это состояние можно спутать с нарастанием недостаточности кровообращения.
При пневмоните – притупление легочного звука, на рентгене – очаги воспаления. Введение ГКС дает быстрый эффект. Если ответ медленный, то дозу можно увеличить в 1,5 – 2 раза с постепенным снижением.
Если течение синдрома Дресслера рецидивирующее, тогда поддерживающая доза 2,5 – 5мг несколько месяцев, антибиотики не назначаются.
Диагноз: ЭХОКГ
Лечение: НПВС короткими курсами, ГКС (30-40 мг)
Ранняя постинфарктная стенокардия
Дает клинику ангинозного приступа. Приступ непродолжительный, ощущения жжения – классический приступ стенокардии. Это состояние увеличивает риск инфаркта миокарда и внезапной смерти.
Диагностика: СКГ, ЭХОКГ
Причины: 1. стеноз артерий в зоне некроза;
2. многососудистое поражение вне зоны некроза;
3. постинфарктное ремоделирование левого желудочка с систолической дисфункцией.
Лечение: при стенозе артерий и при многососудистом поражении - нитраты, гепарин, бета-адреноблокаторы, АКШ. При постинфарктном ремоделировании левого желудочка - ИАПФ, нитраты
Осложнения ЖКТ и почек
У пациента с инфарктом миокарда может случиться:
• Парез кишечника, усиление симптомов диафрагмальной грыжи, икота, рвота
• Кровотечение из острых язв и эрозий. Развернутая клиника может сопровождаться приступами стенокардии, расширением зоны некроза
Лечение: отмена гепарина, кровоостанавливающие ЛС, отмена наркотиков, прозерин, промывание желудка, восполнение жидкости (электролиты, глюкоза), аминазин.
Абдоминальный синдром
• Боль в животе
• Стул неустойчивый
• Иногда появляется рвота с переваренной кровью, кровотечения ЖКТ
• При параличе кишечника возникает вздутие живота, плохое выделение газов, боли распирающего характера
Лечение пареза кишечника:
- Постоянная назо-гастральную аспирация
- Исключить традиционный прием жидкости и пищи через рот
- Назначаются психотропные и седативные лекарственные препараты и отменяют опиаты
Развитие эпигастральных болей при инфаркте миокарда
Боли обусловлены вовлечением в процесс перикарда. Раздражаются диафрагмальный и блуждающий нервы, что вызывает рефлекторные изменения тонуса брюшных мышц, желудка и кишечника.
Психические нарушения
- Соматогенные нарушения возникают из-за гипоксии. Происходит нарушение сознания, бред, галлюцинации), встречается в 2-10%
- Нозогении - 90%
1.гипернозогнозия - это преувеличение тяжести болезни и постоянное эмоционально окрашенное, паническое ожидание «жутких» ее последствий
- Аффективные (депрессии, эйфории), сверхценная ипохондрия, параноидальные реакции.
- Невротические реакции (витальные страхи, панические атаки)
2. Анозогнозия - отсутствие критической оценки больным своего заболевания.
Синдром Дресслера в практике кардиолога и пульмонолога: диагностика на стыке специальностей
Всемирная организация здравоохранения выделила 10 наиболее опасных патологических состояний, к числу которых отнесла коронарную болезнь, уносящую ежегодно более 7 млн жизней. Основная клиническая форма этой болезни, инфаркт миокарда (ИМ), является частой причиной смерти как в Украине, так и во всем мире. В структуре смертности населения нашей страны удельный вес летальных исходов вследствие ИМ составляет 22,5% [1].
Клинический случай
Больной С., 70 лет, поступил в инфарктное отделение 26.01.2016 г. с диагнозом: острый Q-позитивный ИМ задней стенки левого желудочка (ЛЖ). При поступлении предъявлял жалобы на интенсивную боль за грудиной, одышку при ходьбе, тошноту, слабость. В анамнезе гипертоническая болезнь около 30 лет, максимальное артериальное давление (АД) 180/100 мм рт. ст. При поступлении сознание ясное, кожные покровы бледные, пульс ритмичный, тоны сердца приглушены, систолический шум на верхушке, акцент второго тона над аортой, частота сердечных сокращений (ЧСС) 78 в минуту, левая граница относительной тупости сердца расширена влево на 1,5 см. Перкуторно над легкими ясный легочной звук, аускультативно ослабленное везикулярное дыхание, частота дыхательных движений (ЧДД) 16 в минуту. Печень у края реберной дуги, периферические отеки не выявлены.
27.01.2016 г. проведено стентирование инфарктобусловившей коронарной артерии стентом без лекарственного покрытия. В этот же день на рентгенограмме органов грудной клетки, выполненной в вынужденном горизонтальном положении в условиях палаты, были выявлены изменения, вызывающие подозрение на негоспитальную (2-е сутки пребывания в стационаре) правостороннюю пневмонию (рис. 1).

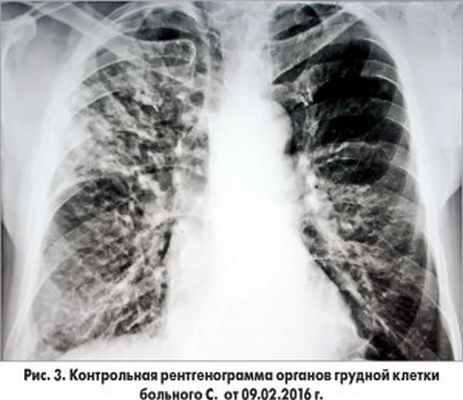
Назначена консультация пульмонолога. Заключение: негоспитальная двухсторонняя пневмония. Назначены антибактериальные препараты: цефипим внутривенно, инфузии левофлоксацина, флюконазол. Через неделю сохранялись кашель со скудной мокротой светло-серого цвета, субфебрилитет; на рентгенограмме органов грудной клетки от 09.02.2016 г. (15-е сутки пребывания в стационаре) – справа без существенной динамики, усилились изменения в левом легком (рис. 3).
Ультразвуковое исследование (УЗИ) сердца показало уменьшение зоны гипокинезии в области задней стенки ЛЖ. На ЭКГ синусовый ритм. В клиническом анализе крови СОЭ 21 мм/ч. У пациента на фоне комбинированной антибиотикотерапии цефалоспорином IV поколения с антипсевдомонадной активностью и фторхинолоном III поколения в течение 7 дней общее состояние не улучшилось, гемодинамика оставалась стабильной, ЧДД 18 в минуту, симптомов интоксикации не было, печень у края реберной дуги, ослабленное дыхание в легких с обеих сторон, отеки не выявлялись. Трактовка изменений в легких как проявлений легочного застоя при прогрессирующей сердечной недостаточности была неубедительной ввиду стабильного клинического состояния больного, отсутствия отеков, увеличения печени и позитивной динамики УЗИ сердца. Пациент дважды был осмотрен фтизиатром, проводились исследования мокроты в лаборатории противотуберкулезного диспансера (мазок, МГ-тест, посев на жидкую среду): микобактерии туберкулеза не найдены, диагноз туберкулеза был исключен.
18.02.2016 г. (24-е сутки пребывания в стационаре) была проведена мультисрезовая КТ органов грудной клетки и средостения с контрастированием, в верхней доле правого легкого выявлена очагово-сливная инфильтрация. Идентичные, менее выраженные участки инфильтрации визуализировались в верхней доле левого легкого. В нижних отделах – пневмофиброз. В правой плевральной полости – небольшое количество свободной жидкости толщиной до 8 мм, в левой плевральной полости – свободная жидкость толщиной до 20 мм, в перикарде – небольшое количество жидкости. Сосуды проходимы, не расширены, признаков тромбоэмболии ветвей легочной артерии не выявлено (рис. 4).

Таким образом, данные КТ органов грудной клетки и отсутствие изменений в системе гемостаза позволили исключить диагноз ТЭЛА. Пациенту была назначена комбинация петлевого диуретика с блокатором рецепторов альдостерона (торасемид с эплереноном) на фоне продолжающегося лечения ацетилсалициловой кислотой, клопидогрелем, аторвастатином, эналаприлом, бисопрололом, пантопразолом, цефипимом. Состояние больного было стабильным, сохранялся небольшой кашель, температура тела нормализовалась, антибиотики были отменены, однако на рентгенограмме органов грудной клетки от 20.03.2016 г. (55-е сутки наблюдения) оставались признаки перикардита, плеврального выпота и изменений в легких (рис. 5).

Пациент продолжал получать ацетилсалициловую кислоту, клопидогрель, аторвастатин, эналаприл, бисопролол, пантопразол, эплеренон. На рентгенограмме от 4.04.2016 г. (70-е сутки наблюдения) отмечалась выраженная положительная динамика в виде рассасывания инфильтративных изменений в легких и исчезновения плеврального выпота (рис. 6).

Таким образом, у больного через сутки от момента возникновения острого ИМ, вероятнее всего, развился синдром Дресслера, что не было типичным в отношении сроков возникновения этого осложнения. Однако в клинической картине преобладал типичный симптомокомплекс – пневмонит, плеврит, перикардит. Отсутствие динамики изменений в легких на фоне длительной антибиотикотерапии при одновременном отсутствии симптомов интоксикации ставили под сомнение диагноз пневмонии. Были исключены ТЭЛА и наличие туберкулезного процесса. Отсутствие одышки, тахикардии, ухудшения ультразвуковой симптоматики при эхокардиографии и стабильная гемодинамика не позволяли трактовать наличие выпота в полости перикарда и плевральных полостях как проявление нарастающей сердечной недостаточности. Отсутствие артралгий, скованности движений в суставах, повышения температуры тела, лабораторные данные не вызывали подозрений на развитие системного заболевания соединительной ткани. Длительность изменений в легких, перикардита и двухстороннего плеврита (более 2 мес), как и сроки возникновения, также были нетипичными для синдрома Дресслера. Однако связь заболевания с острым ИМ, исключение основных патологических состояний, с которыми проводится дифференциальная диагностика синдрома, наличие классической триады симптомов – плеврита, пневмонита, перикардита – и их исчезновение на фоне приема препаратов кардиогруппы с большой долей вероятности могли демонстрировать картину постинфарктного синдрома Дресслера.
Список литературы находится в редакции.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Сьогодні в рамках оцінки чинників ризику серцево-судинних (СС) захворювань дедалі більший інтерес наукового світу прикутий до ендотелію та його функції. Ендотелій уражається насамперед унаслідок артеріальної гіпертензії (АГ), це проявляється розвитком його дисфункції та морфологічною перебудовою артеріальної стінки. Добре відомо, що з віком підвищується судинна жорсткість, що пов’язують зі зниженням в артеріальній стінці вмісту еластину та підвищенням кількості колагену 3. У разі АГ перебіг цих процесів значно прискорюється – судинний вік починає випереджати хронологічний (паспортний). Тому дедалі більше науковців для опису функціонального та морфологічного стану серцево-судинної системи використовують термін «синдром раннього старіння судин», або EVA‑синдром (early vascular aging), як модель старіння судин, яка більш точно відображає структурні та функціональні зміни, що відбуваються в організмі в міру його старіння [1].
Ішемічна хвороба серця (ІХС) є провідною причиною інвалідизації та смертності від серцево‑судинних захворювань (ССЗ). У розвинених країнах Європи на 1 млн населення припадає 30-40 тис. хворих, які страждають на ІХС [1]. До того ж немає пояснень для показників смертності українських чоловіків і жінок, які в 14 і 23 рази більше, ніж у Франції [2]. Крім базисної терапії пацієнтів з ІХС, потенційним напрямом лікування є застосування підходів, які здатні покращити енергозабезпечення кардіоміоцитів, мікроциркуляцію та функцію ендотелію судин [3].
COVID‑19 чинить суттєвий негативний вплив на серцево-судинну (СС) систему. Наявні у пацієнтів серцево-судинні захворювання (ССЗ) до інфікування COVID‑19 та вірусне навантаження асоційовані з пошкодженням міокарда й гіршими результатами. Пандемія триває, зокрема, з’являються нові варіанти коронавірусу, тож розуміння патофізіології та відповідних клінічних наслідків допоможе розширити уявлення про основні механізми розвитку хвороби. Вирішальне значення також мають встановлення нових біомаркерів СС-ускладнень і розробка ефективних методів лікування COVID‑19. Пропонуємо до вашої уваги консенсусний документ Європейського товариства кардіологів (ESC) та Асоціації невідкладної кардіологічної допомоги (ACVC) у співпраці з Європейською асоціацією серцевого ритму (EHRA) 2021 р., у якому підсумовано сучасні відомості про ураження СС-системи на тлі COVID‑19 та його постгострі наслідки. .
Незважаючи на сучасні методи відновлення коронарного кровотоку, показники смертності після перенесеного гострого коронарного синдрому (ГКС) залишаються досить високими, що пов’язують з ушкодженням міокарда під час реперфузії. Відповідно до сучасних уявлень, провідною причиною цього явища є ішемічний каскад, який може запускати процеси загибелі кардіоміоцитів і бути відповідальним за 50% кінцевого розміру зони некрозу при ГКС, виникнення реперфузійних аритмій, систолічної мікросудинної дисфункції. Саме тому адекватне блокування ішемічного каскаду, спрямоване на елімінацію активних форм кисню, активацію антиоксидантів, на сьогодні вважається важливою складовою менеджменту пацієнтів із ГКС. .
Читайте также:
