Послеоперационные осложнения пневморетинопексии. Профилактика
Обновлено: 03.05.2024
В хирургии катаракты при псевдоэксфолиативном синдроме Результаты УБМ-исследований со всей очевидностью показали возможность диагностирования ПЭС на доклинических и ранних клинических стадиях патологического процесса с объективным морфологическим точным определением дистрофических изменений связочного аппарата хрусталика, включая наличие, локализацию и протяженность разрыва волокон цинновой связки.
Полученные данные позволили внести коррекцию в тактику офтальмохирурга при факоэмульсификации катаракты, расширить показания к ее использованию, лимитировать ситуации вынужденного перехода на интракапсулярные методы.
Ретроспективный анализ 135 операций, выполненных с учетом предоперационных результатов УБМ-исследований, представляет, с нашей точки зрения, несомненный интерес для практикующих офтальмохирургов.
При I стадии ПЭС по УБМ-исследованиям (17 операций) клинические проявления ПЭС отсутствовали у подавляющего большинства больных (13 случаев).
У всех больных данной группы представлялось возможным добиться медикаментозного мидриаза инстилляциями мидриатиков. Факоэмульсификация выполнялась без ограничений в рамках «ирригация-аспирация» с диапазоном ультразвуковой энергии в зависимости от плотности ядра от 30 до 80%. Все операции прошли без осложнений.
При II стадии ПЭС по УБМ (65 операций) клинические признаки патологии отсутствовали в 26 случаях и соответствовали I стадии по биомикроскопии — в 10 случаях и II стадии — на 29 глазах.
Диафрагмальная функция радужки была нарушена у 43 из 65 больных данной группы, что потребовало инъекций мидриатиков для достижения медикаментозного мидриаза перед операцией.
При III стадии ПЭС по УБМ (34 операции) симптомы ПЭС при биомикроскопии отсутствовали в 17 случаях, соответствовали I стадии — 2 глаза и II стадии — 15 глаз. Отмечались резкая атрофия радужки и нарушения ее дифрагмальной функции, симптомы иридо- и факодонеза имели место в 8 из 34 случаев.
Инстилляциями и инъекциями мидриатиков удалось добиться должного мидриаза (не менее 5 мм) у большинства больных данной группы. Лишь в 3 случаях встала необходимость в проведении сфинктеротомии и в 2 случаях — использовании ирис-ретракторов для создания оптимальных условий выполнения факоэмульсификации.
Аналогично предыдущей группе факоэмульсификация выполнялась с максимальной деликатностью манипуляций, на щадящих режимах ирригации-аспирации при дробной подаче ультразвука. Во всех случаях использовано внутрикапсульное кольцо, которое вводилось инжектором после выполнения переднего капсулорексиса и гидродиссекции вискоэластиком. Гидроделинеация выполнялась путем осторожного введения вискоэластика по различным секторам капсульного мешка, таким образом предотвращая тракции на волокна цинновой связки.
Разрыв капсулы хрусталика имел место в 2 случаях без выпадения стекловидного тела. Наличие кольца обеспечивало натяжение экваториального свода капсульного мешка, облегчало манипуляции по аспирации остаточных хрусталиковых масс с использованием технологии «локальной» аспирации и ирригации (13). Натяжение капсульного мешка кольцом позволяло осуществить успешную имплантацию заднекамерных интраокулярных линз.
При IV стадии по УБМ (19 операций) выявлены различной протяженности разрывы волокон цинновой связки в одном или нескольких сегментах и в 4 случаях — по всей окружности связочного аппарата хрусталика.
Следует отметить, что клинические признаки дислокации хрусталика (иридодонез, факодонез, измельчение глубины передней камеры) были диагностированы в этой группе при биомикроскопии в 8 из 19 случаев (42%). Выявленные изменения указывали на необходимость дифференцированного подхода к хирургической тактике.
При нарушении волокон цинновой связки до 3 сегментов (15 операций) факоэмульсификация выполнялась аналогично предыдущей стадии с обязательным введением интракапсулярного кольца. Факофрагментация ядра осуществлялась после предварительной фиксации блока «радужка — передняя капсула — кольцо» на четырех ирис-ретракторах(рис. 4.10).
В 4 случаях принято решение о выполнении интракапсулярной экстракции катаракты. Перед удалением хрусталика передняя камера углублялась вискоэластиком. Заполнение передней камеры вискоэластиком облегчало манипуляции и при введении интраокулярной линзы. Выпадение стекловидного тела имело место в 2 случаях.
У подавляющего числа больных операции (95,6%) и ранний послеоперационный период (93,3%) протекали неосложненно. Во время операции имели место осложнения в 6 (4,4%) случаях (разрыв задней капсулы, выпадение стекловидного тела и геморрагические осложнения) (табл. 4.3). Гипертензия (4,4%) и экссудативная реакция (2,2%) отмечены в первые дни после операции. Осложнения в ходе операции имели место у наиболее тяжелого контингента больных с обширным лизисом волокон цинновой связки. Своевременная диагностика нарушения связочного аппарата хрусталика, протяженности разрыва волокон цинновой связки позволили свести к минимуму осложнения и осуществить планируемую интраокулярную коррекцию.
Через 1-3 года после операции обследованы 93 пациента. При отсутствии исходной патологии зрительного нерва и сетчатки высокая острота зрения отмечена у большинства больных: 0,5-1,0 в 94% случаев. При биомикроскопии отмечалось равномерное натяжение капсульного мешка, центральное стабильное положение ИОЛ.
Таким образом, ультразвуковая биомикроскопия позволяет педантично визуализировать структуры переднего сегмента глаза, недоступные при биомикроскопии, определить симптомы и их совокупность, дающие возможность более объективно констатировать характер и степень дистрофических изменений при псевдоэксфолиативном синдроме.
С помощью УБМ представилась возможность диагностировать ПЭС при отсутствии клинической симптоматики в 41,5% случаев (56 из 135). Начальные признаки несостоятельности связочного аппарата хрусталика (II стадия по УБМ), не выявленные клинически, обнаружены 48,1% обследованных больных (65 случаев из 135). Разрыв волокон цинновой связки (III и IVстадии по УБМ) диагностирован в 39,3% вместо 11,8% случаев по результатам биомикроскопии. Объективная диагностика состояния связочного аппарата хрусталика, визуализация при УБМ протяженности разрыва волокон цинновой связки легли в основу выбора оптимальной методики факоэмульсификации и, тем самым, позволили обеспечить профилактику операционных осложнений у большинства из них. При этом существенно лимитированы показания интракапсулярной экстракции катаракты (4 случая из 135).
Результаты выполненных исследований могут быть суммированы следующими положениями.
Ультразвуковая биомикроскопия является объективным и высокоинформативным методом диагностики псевдоэксфолиативного синдрома, обеспечивая:
• доклиническую диагностику патологического процесса в 41,5% случаев:
•выявление несостоятельности связочного аппарата хрусталика при отсутствии признаков при биомикроскопическом исследовании (48,1%);
•диагностику разрыва волокон цинновой связки с визуализацией его протяженности (39,3%);
• диагностику нарушений пространственных соотношений структур переднего сегмента глаза, недоступную оптической биомикроскопии.
В зависимости от интенсивности, акустической плотности включений, их локазации, состяния волокон цинновой связки и нарушения анатомо-топографических структур переднего сегменто глаза выделено 4 стадии ПЭС по УБМ, каждая из которых отражает последовательные этапы развития патологического процесса.
Найдены объективные признаки УБМ-диагностики разрыва волокон цинновой связки, позволяющие оценить степень патологии и протяженность повреждения связочного аппарата хрусталика.
Псевдоэксфолиативный синдром отражает патологию обоих глаз, не зависит от рефракции, прогрессирует с возрастом и обнаруживается практически у всех больных с глаукомой в возрастной группе старше 60 лет.
Имбибиция структур переднего сегмента глаза эксфолиациями и нарушение их пространственных соотношений при выраженных проявлениях заболевания (III и IV стадии по УБМ) могут расцениваться как один из патологических механизмов гипертензии и глаукомы при ПЭС.
Диагностика состояния волокон цинновой связки по данным УБМ определяет выбор метода хирургии катаракты и особенности техники проведения факоэмульсификации.
Использование внутрикапсульного кольца, рекомендуемого режима аспирации-ирригации, бимануальная техника, формирование блока «радужка-передний капсулорексис-интракапсулярное кольцо» расширяют показания к факоэмульсификации при лизисе волокон цинновой связки протяженностью до 2/3 по окружности у пациентов с ПЭС.
Послеоперационные осложнения пневморетинопексии. Профилактика
Послеоперационные осложнения пневморетинопексии. Профилактика
Послеоперационные осложнения пневморетинопексии:
- Новые/пропущенные разрывы 7-33%
- Разблокирование разрыва 0-14%
- Эпиретинальная мембрана 2-11%
- Пролиферативная витреоретинопатия 3-13%
- Катаракта 0-20%
- Кистозный макулярный отек 0-8%
- Замедленная абсорбция субретинальной жидкости 0-6%
- Макулярное отверстие 0-3%
- Передняя ишемическая нейрооптикопатия 0-2%
- Эндофтальмит

Наиболее частое послеоперационное осложнение пневморетинопексии - это новые и/или пропущенные разрывы сетчатки. Большинство из них выявляются в течение первого месяца после операции, что составляет от 61 до 86%. Из новых и/или пропущенных разрывов 76% обнаруживаются в верхних двух третях сетчатки. Они почти всегда располагаются кпереди от экватора и чаще встречаются в артифакичных или афакичных глазах. Пропущенных разрывов можно избежать путем очень тщательного предоперационного обследования сетчатки.
Авторы считают, что для обнаружения мелких разрывов перед операцией очень полезно обследование периферии сетчатки с линзой 78 дптр или 90 дптр. Кроме того, случаи с помутнениями сред, такими как секторальная или спицеобразная кортикальная катаракта, периферические помутнения капсулы и гемофтальм, препятствующими ясной визуализации, хуже подходят для пневморетинопексии.
Риск появления новых разрывов минимизируется путем профилактической лазеркоагуляции всех подозрительных изменений, таких как решетчатая дегенерация, кистозные пучки и меридиональные комплексы, перед введением газа. Следует иметь в виду профилактическую круговую лазеркоагуляцию в области базиса стекловидного тела, которая по некоторым данным снижает частоту новых/пропущенных разрывов и увеличивает хирургический успех. Замедленная резорбция субретинальной жидкости встречается от 0 до 6% случаев. В большинстве случаев первоначальная отслойка была подострой или хронической, и субретинальная жидкость, оттесненная от первичного разрыва, оказывалась «запертой» в субретинальном пространстве.
Другие описанные послеоперационные осложнения включают образование эпиретинальных мембран в 0-11% случаев, ПВР - в 3-13%, кистозный макулярный отек - в 0-8%, макулярное отверстие - в 0-3%, переднюю ишемическую нейрооптикопатию - в четырех случаях и эндофтальмит - в одном случае.
Поздние осложнения со стороны переднего сегмента представлены образованием катаракты. Хотя повреждение хрусталика во время инъекции встречается редко, поздняя катаракта, предположительно вследствие контакта газа с хрусталиком, наблюдается гораздо чаще. Катаракта встречается в 0-20% случаев, частота зависит от типа и количества применяемого газа, а также от длительности послеоперационного наблюдения.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Послеоперационные осложнения пневморетинопексии. Профилактика
В данной статье отмечена актуальность, распространенность и последствия такого заболевания, как возрастная макулярная дегенерация. Авторами представлены результаты сравнительного анализа эффективности различных видов лечения влажной формы возрастной макулярной дегенерации. Показано, что при выборе тактики лечения больных данной патологией необходимо учитывать клиническую форму и стадию течения заболевания. Даны рекомендации по лечению возрастной макулярной дегенерации в зависимости от формы и стадии заболевания. При влажной форме возрастной макулярной дегенерации показано проведение хирургического лечения в виде пневморетинопексии с последующим проведением лазерного барража макулярной зоны, что обеспечивает более высокие результаты лечения, в то время как традиционное лечение ингибиторами ангиогенеза влажной формы возрастной макулярной дегенерации не обеспечивает стабильных клинико-функциональных результатов.
1. Будзинская М.В. Субретинальная неоваскулярная мембрана при возрастной макулярной дегенерации // Вестн. офтальмол. - 2006. - № 4 - С. 49-54.
2. Егоров Е.А. Современные направления в лечении инволюционной центральной хориоретинальной дистрофии / Е.А. Егоров, Д.В. Кац, Т.О. Елисеева, М.В. Ермакова // Актуальные вопросы терапии. -2006.- № 5- С. 2-6.
4. Столяренко Г.Е. Первый опыт трансвитреальной хирургии центральной хориоретинальной дистрофии, осложненной экссудативной отслойкой сенсорной сетчатки и пигментного эпителия // Вестн. офтальмол. - 1989. - № 4.- С. 6-9.
5. Algvere P.V. Transpupillary thermotherapy of occult CNV with no or minimally classic CNV in age-related macular degeneration // Semin. Ophthalmol.- 2001. -Vol. 16.- P. 90-96.
6. Holz F.G., Pauleikohoff D. Altersabhangige makuladegeneration // Springer Verlag. - 2004. – Р. 240
Возрастная макулярная дегенерации сетчатки (ВМД) занимает одно из первых мест среди причин слепоты у лиц старше 60-ти лет и являются ведущей причиной потери центрального зрения в развитых странах [2,6,7]. В последние годы данная патология диагностируется не только в пожилом, но и у лиц относительно молодого возраста, обусловливая первичную инвалидизацию в 11% случаев у лиц трудоспособного возраста, и в 28% случаев у пожилых.
По данным Всемирной Организации Здравоохранения, число людей старше 60-ти лет к 2050 году увеличится втрое, при этом, возрастет доля населения старшей возрастной группы, которая на сегодня в экономически развитых странах составляет около 20% [7]. В России заболеваемость ВМД составляет более 15 человек на 1000 населения [1,2].
В настоящее время, различают две основные клинические формы ВМД: «сухую», или неэкссудативную форму с преобладанием ретинальных друз, дефектов и участков атрофии пигментного эпителия, и «влажную», или экссудативную форму с наличием экссудативной отслойки пигментного и нейроэпителиального слоев сетчатки, субретинальной неоваскуляризации [6,7].
Влажные формы ВМД являются прогностически наиболее неблагоприятными и ведут к резкому и значительному, вплоть до светоощущения, снижению центрального зрения. Серозная экссудативная отслойка пигментного эпителия представляет особый интерес, поскольку является неким переходным периодом между этапом постепенного снижения остроты зрения и быстрой, необратимой утратой центрального зрения. С одной стороны, экссудативные изменения могут сохраняться в стабильном состоянии достаточно долго, а при экстрафовеальной локализации даже практически не влиять на остроту зрения. Более того, при отсутствии лечения у 19 % больных отслойки пигментного эпителия могут спонтанно прилегать. С другой стороны, при отсутствии прилегания сетчатки у 61,9 % пациентов в течение 1 года формируется субретинальная неоваскулярная мембрана [3,4,5].
Разнообразие клинических проявлений ВМД, а также отсутствие единого мнения о причинах возникновения и развития заболевания затрудняют разработку эффективных патогенетически обоснованных методов лечения и профилактики данной патологии.
Цель исследования - оценка эффективности различных методов лечения влажной формы ВМД.
Материалы и методы
Клинические исследования проведены у 57 больного (57 глаз) с различными стадиями влажной формы ВМД. Пациенты были разделены на 2 группы в зависимости от степени тяжести заболевания:
- 1-я группа - 34 человека (34 глаза) с экссудативной отслойкой сетчатки различной степени выраженности на фоне влажной формы ВМД;
- 2-я группа - 23 человека (23 глаза) с локальной отслойкой пигментного эпителия и макулярным отеком сетчатки с субретинальной неоваскуляризацией на фоне влажной формы ВМД.
Пациентам 1-й группы выполнялось хирургическое лечение по разработанной нами методике, включающей проведение пневморетинопексии сетчатки в комбинации с лазерным барражем макулярной зоны (патент РФ на изобретение № 2230537 от 20.06.2004 «Способ хирургического лечения экссудативной сенильной макулодистрофии»). Больным 2-й группы выполнялись интравитреальные инъекции препарата Луцентис (ИВВЛ) по стандартной схеме для ВМД.
Всем пациентам перед операцией проводили офтальмологическое обследование, включавшее визометрию, периметрию, биомикроскопию переднего отрезка глаза, обратную офтальмоскопию, пневмотонометрию, электрофизиологические исследования (фосфен, лабильность зрительного нерва, электроокулографию), оптическую когерентную томографию (ОКТ). В послеоперационном периоде в ходе динамического наблюдения проводили визометрию, периметрию, тонометрию. Лечение пациентов 1-й и 2-й групп в послеоперационном периоде проводили по стандартной схеме, включавшей инстилляции растворов антибиотиков и кортикостероидов.
Статистическую обработку проводили с применением программы «STATISTICA» с предварительной оценкой характера распределения и использованием непараметрического критерия Уилкоксона и Манна-Уитни.
Результаты
Клинические исследования проведены у 57 больных (57 глаз) с различными стадиями влажной формы ВМД. Среди обследованных пациентов было 32 (54,9%) женщин и 25 (45,1%) мужчины. Возраст больных варьировал от 54 до 75 лет (в среднем 67 лет).
1-ю группу составили 34 человек (34 глаза), из них 19 (64,2%) женщин и 15 (35,8%) мужчин в возрасте от 58 до 74 лет (в среднем 60,43 лет). По степени выраженности патологических изменений на глазном дне было 26 (42,8%) человек с центральными экссудативными отслойками пигментного и нейроэпителия сетчатки от 2 до 4 размеров диска зрительного нерва, в 6 (14,6%) случаях имела место экссудативно-геморрагическая отслойка сетчатки, в 2 (7,4%) - макулярный разрыв сетчатки.
2-ю группу составили 23 человека (23 глаза), из них 15 (65,2%) женщин и 8 (34,8%) мужчин в возрасте от 54 до 75 лет (в среднем 65,9 лет). У всех пациентов данной группы (100%) диагностированы отек и/или локальная (в пределах 2 размеров диска зрительного нерва) отслойка пигментного эпителия сетчатки или классическая хориоидальная неоваскуляризация (ХНВ).
Кровоизлияния в сетчатку и субретинальное пространство различной степени выраженности до лечения обнаруживались у больных, в 1-й группе - в 14,6% (6 глаз), в 3-й группе - в 18,6% (8 глаз).
Результаты исследования зрительных функций
У больных 1-й группы после комбинированного лечения, включающего проведение пневморетинопексии с последующей лазеркоагуляцией сетчатки, острота зрения в течение первого месяца возросла в среднем на 0,06 (±0,03), и в последующем сохранялась на достигнутом уровне в течение всего периода наблюдения - 12 мес. (табл. 1).
Таблица 1
Динамика остроты зрения у больных влажной формой ВМД в зависимости от вида лечения
Операции на сетчатке глаза: особенности послеоперационного периода
Сетчатка — зрительный анализатор, который отвечает за фокусировку световых лучей, проходящих через роговицу и хрусталик глаза. Она передает полученное изображение на зрительный нерв. От того, насколько правильно функционирует эта часть глаза, зависит четкость видимости предметов. К сожалению, далеко не всегда удается избежать проблем с сетчаткой: она отслаивается от расположенного под ней сосудистого слоя, разрывается или истончается, что грозит полной потерей зрения.
В офтальмологии разработано несколько видов операций на сетчатке. Это малоинвазивные или классические хирургические вмешательства, целью которых становится предотвращения слепоты или восстановление зрения. Выбор вида операции зависит от степени повреждения тканей, причин их возникновения, сопутствующих патологий и возраста пациента.
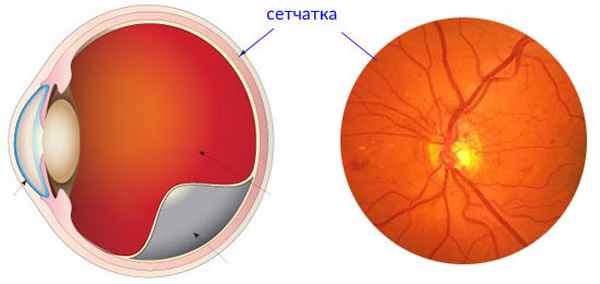
Разновидности операций на сетчатке
В хирургической офтальмологии принято разделение операций на сетчатке на два типа:
- Плановые вмешательства — процедуры, которые проводят в удобное для пациента время. Их применяют в ситуациях, когда патологический процесс относительно стабилен, нет риска стремительного прогресса и резкого ухудшения состояния. Плановые операции на глазах проводят при неосложненной отслойке сетчатки без признаков ее разрыва или дистрофии.
- Срочные вмешательства — процедуры, которые проводят в максимально сжатый период после постановки диагноза. Такие операции показаны при осложненных заболеваниях сетчатки с высоким риском кровоизлияния, разрыва, инфицирования и т. д. Их проведение назначают на ближайшие сутки или 2-3 дня.
Официальная классификация процедур делит их на классические хирургические или микрохирургические вмешательства и малоинвазивные процедуры. Классическая операция на сетчатке проводится через небольшие разрезы на оболочке глаза. Они используются для укрепления и восстановления поврежденных участков сетчатки. Мини-инвазивные операции делают без нарушения целостности роговицы и других структур глаза. Проводятся они с помощью лазерных, волновых и лучевых технологий.
Обе группы вмешательств, проводимых с применением современной аппаратуры, показывают эффективность свыше 95%. Единственное, чем они отличаются, — продолжительностью послеоперационного периода. После малоинвазивной процедуры он длится не дольше месяца и почти не требует реабилитации, а после обычной операции — до полугода со множественными ограничениями.
Пломбирование сетчатки
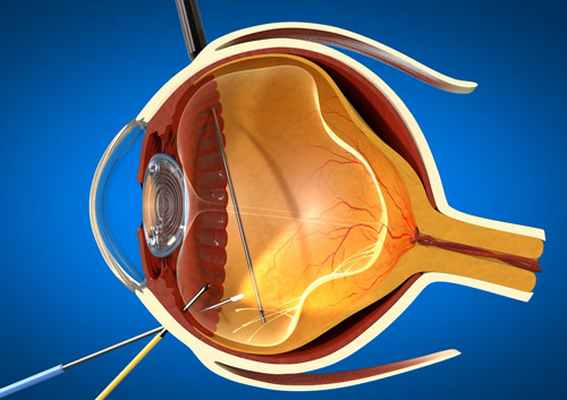
Пломбирование сетчатки — классическое хирургическое вмешательство, целью которой становится сокращение пространства между оболочками глаза. Применяется при отслоении сетчатки, сопровождающимся накоплением под ней экссудата (жидкости).
Пломбирование проводится с помощью силиконовой губки, которая вводится в полость глаза и устанавливается над местом отслойки. В зависимости от локализации патологического очага пломбирование может быть:
- радиальным — с помещением губки по линии, идущей от центра сетчатки к ее краю. Используется при отслоении незначительного фрагмента сетчатки;
- секторальным — с размещением губки на клиновидном участке, узкая часть которого располагается по центру сетчатки, а широкая – по ее краю. Используется при отслоении достаточно крупного фрагмента ткани;
- круговым — с помещением губки на обширном участке сетчатки, используется при обширном отслоении.
Пломбирование помогает предотвратить разрыв внутренних оболочек глаза и создает давление, необходимое для удаления жидкости из-под сетчатки. Со временем этот слой срастается с лежащим ниже сосудистым дном.
Этапы операции:
- Подготовка. Проводится обследование сетчатки и выяснение точных размеров, формы и локализации отслоившегося фрагмента. За неделю до операции делают анализы крови для выявления возможных противопоказаний. По снятым меркам изготавливают силиконовую пломбу.
- Перед операцией пациент укладывается на хирургический стол, ему вводят анестезию.
- Хирург-офтальмолог делает надрез на конъюнктивальной оболочке, устанавливает дренажную систему для поддержания стабильного давления в глазу и профилактики попадания в его полость воздуха.
- Через разрез имплантируется губка, устанавливается на место отслойки и фиксируется швами.
- Из полости глаза удаляется лишняя жидкость, при необходимости вводится небольшой объем специальной газовой смеси, чтобы пломба плотно прилегала к сетчатке.
- На оболочку глаза накладываются швы.
Такая операция предотвращает дальнейшее развитие патологии и полностью сохраняет стекловидное тело при осложненных заболеваниях органов зрения. Ее недостаток — невозможность на 100% восстановить утраченное зрение и наличие неприятных последствий: ослабление мышц, отвечающих за движения глаз, повышение внутриглазного давления и катаракта.
Баллонирование сетчатки
Баллонирование — хирургическая процедура, которая используется для устранения неосложненного отслоения сетчатки. Показанием к ней считается локализованный дефект без признаков разрыва слоя и излияния крови в стекловидное тело. В процессе используется миниатюрное устройство, состоящее из баллона, наполняемого жидкостью.
Как проходит операция:
- Пациент укладывается на хирургический стол, ему вводят анестезию и после того, как она подействует, делают небольшой надрез на оболочке глаза в месте ее соприкосновения с конъюнктивой.
- В разрез вводят миниатюрный гибкий катетер с баллоном. Когда его конец достигнет места отслойки, врач высвободит баллон и разместит его над дефектом.
- После стабилизации баллона его наполняют жидкостью. Увеличившись в объеме, он прижимает сетчатку к подлежащему сосудистому слою.
- После фиксации сетчатки баллон опустошают и выводят с помощью катетера. Для дополнительного закрепления врач может использовать лазерную коагуляцию.
- На надрез накладывают шов.

Эффективность этой операции очень высока, однако применяется она все реже. Причина — затянутый послеоперационный период и высокая вероятность образования гематомы внутри глаза. Также для такой операции характерно отдаленное осложнение — катаракта.
Операция по замене сетчатки
Имплантация сетчатки — сравнительно новый вид хирургического вмешательства в офтальмологии. С его помощью восстановление зрения возможно даже при необратимой слепоте, возникшей на фоне разрыва, обширной дистрофии и отслойки сетчатки, а также при потере зрения вследствие заболеваний зрительного нерва.
Благодаря установке имплантата удается вернуть человеку способность видеть контуры предметов, различать источники света и цвета. Вернуть 100% зрение искусственные материалы не способны.
В настоящее время имплантация сетчатки находится на стадии клинических испытаний, поэтому недоступна.
Операции на укрепление сетчатки
Профилактическое укрепление — стандартная малоинвазивная операция на сетчатке, которую проводят пациентам с предрасположенностью к отслойке и высоким риском разрыва ретины. Она направлена на уменьшение вероятности проблем со зрением в будущем. При неосложненных патологиях они используются как терапевтические процедуры — для точечного «припаивания» ткани к сосудистому слою.
Выполняется укрепление тремя способами:
Криопексия — воздействие на ретину сверхнизкими температурами.
Лазерная коагуляция — точечное воздействие на сетчатку лазерным лучом.
Пневморетинопексия — процедура с использованием газа.
Метод криопексии используется при риске отслойки или дистрофии ретины на фоне сильно выраженной близорукости. Процедура проводится с местным обезболиванием в амбулаторных условиях. Недостаток методики — эффективен только при небольших и свежих дефектах.

Лазерная коагуляция — более универсальный метод, который используется при всех видах и формах отслоения и разрыва сетчатки. В зависимости от типа патологии существует несколько видов процедуры:
- барьерное восстановление сетчатки используется при центральном отслоении;
- пантеринальное — методика, подходящая для устранения обширной отслойки;
- периферическое — профилактическая процедура, в процессе которой коагуляцию проводят точечно в наиболее «слабых» местах сетчатки;
- фокальное восстановление — применяется при небольших отслоениях и разрывах.
Это самый доступный, быстрый и малотравматичный способ восстановления сетчатки без надрезов и проникновения внутрь глазного яблока. Процедура проводится бесконтактно с помощью специальной лазерной установки.
Пневморетинопексия считается наиболее травматичной методикой укрепления сетчатки. Операция проводится под общим наркозом с использованием шприца, наполненного газом. Его вводят над местом отслоения, чтобы вернуть сетчатку на место. Через несколько часов для закрепления эффекта проводят лазерную коагуляцию. Серьезный недостаток метода — чрезмерно длинный послеоперационный период после операции на сетчатке глаза, который достигает полугода.
Особенности восстановительного периода
Восстановление после любого вмешательства на органах зрения определяет успешность операции. Так как ретина относится к высокоорганизованным нервно-сосудистым тканям, для ее «настройки» на правильное функционирование после восстановления требуется время, а также отсутствие факторов, способных свести на «нет» усилия врача. Именно поэтому пациентам, прошедшим лечение, назначается комплексная реабилитация, требующая изменения образа жизни, питания, режима труда и отдыха на определенный период.
Основные особенности в послеоперационный период:
- Максимальное сохранение покоя для глаз в первые дни.
- Постепенная нагрузка и «тренировка» сетчатки в поздних периодах для возвращения способности видеть предметы.
- Соблюдение норм асептики для профилактики инфекционных осложнений до полного восстановления оболочек глаза.
- Рациональное распределение нагрузки на глаза для профилактики повторного развития патологий.
Продолжительность восстановления также зависит от вида операции на сетчатке. Самые короткие сроки требуются после укрепления сетчатки лазером или жидким азотом — от 10 до 14 дней. Чуть больше времени на восстановление требует баллонирование и пневморетиноскопия — до 4 недель. Самые травматичные операции — пломбирование сетчатки и имплантация — требуют полугодового восстановления.
Ранняя и поздняя реабилитация
Весь восстановительный период делится на два этапа:
- Ранний — первый месяц после операции.
- Поздний — с 30 дня после вмешательства до полного восстановления тканей.
На раннем этапе особое внимание уделяется асептике прооперированного глаза, особенно если процедура носила классический хирургический характер. Пациенту назначают:
- инстилляции растворов с антибиотиками для профилактики инфекций;
- прием или закапывание в глаза противовоспалительных средств;
- использование капель для снятия напряжения в глазах.
В первые сутки лекарства используют через 3-4 часа, а затем, по мере заживления тканей, доводят до 1 закапывания капель в сутки.
Также ранняя реабилитация подразумевает предохранение глаз от чрезмерной нагрузки. На этом этапе восстановления пациенту приходиться соблюдать максимум рекомендаций, влияющих на образ жизни: не наклоняться, не принимать ванну, не умывать лицо водопроводной водой и т. д.
Поздний восстановительный период требует более активного включения прооперированного глаза в работу. На этом промежутке врач советует комплекс упражнений для глаза, помогающих восстановить тонус мышц, регулировать направление и «дальность» взгляда. Некоторые ограничения сохраняются, чтобы не допустить перенапряжения или травмирования сетчатки. Продолжаться он может до полугода, иногда чуть дольше.
Ограничения после операции
Кроме защиты глаз от попадания механических частиц и чрезмерной нагрузки светом, после операции важно уделить внимание правильному кровоснабжению прооперированного органа зрения. Чтобы не было быстрых и отдаленных негативных последствий, после вмешательства пациентам нельзя провоцировать приток крови к голове. Для этого нужно избегать:
- жарких и душных помещений, воздерживаться о посещения бани и сауны;
- физического и эмоционального напряжения;
- наклонов вперед, нахождения в положении лежа с запрокинутой головой и сон на стороне, где был прооперирован глаз;
- полетов на самолете;
- погружений под воду.
Также следует избегать перенапряжения глаз, которое возникает при длительном просмотре телевизора, работе за компьютером, нахождении под ярким солнцем. Если обстоятельства требуют работы с мониторами и чтения мелкого шрифта, следует каждые 30 минут смотреть вдаль или отдыхать с закрытыми глазами. В ясные дни надо носить солнцезащитные очки.
Том 7, № 4 (2014)

В статье представлены результаты хирургического лечения катаракты у пациентки с неправильным астигматизмом на фоне сопутствующей патологии роговой оболочки. Авторами продемонстрирована эффективность и безопасность метода коррекции остаточного астигматизма с помощью имплантации добавочной псевдофакичной ИОЛ Sulcoflex (Rayner, Великобритания).
Имплантация клапана Ahmed: интраоперационные и ранние послеоперационные осложнения
Аннотация
Влияние витрэктомии на состояние сетчатки у пациентов с влажной формой возрастной макулярной дегенерации
Аннотация
Опыт хирургии рецидивов отслойки сетчатки после эписклеральных вмешательств
Аннотация
В хирургическом лечении отслойки сетчатки существуют два основных метода - экстрасклеральное и интравитреальное вмешательства. Единого подхода к лечению этой сложной патологии не существует. Цель работы - определить дифференцированную хирургическую тактику и оценить результаты экстрасклеральной хирургии по поводу регматогенной отслойки сетчатки на основе клинико-статистического анализа за пять лет. Результаты показали, что первичная регматогенная отслойка сетчатки с пролиферативной витреоретинопатией (ПВР) стадии А является показанием к эписклеральному пломбированию, при условии, если разрывы располагаются на периферии. Проблемы эписклеральной хирургии, не всегда требующие витреоретинальной хирургии: сочетание периферических разрывов с макулярным отверстием, множественные разрывы, большие клапанные разрывы. Возможные пути оптимизации: применение пневморетинопексии, а при необходимости - дренирование субретинальной жидкости, отказ от криоретинопексии. Причинами 19 рецидивов, потребовавших последующего витреоретинального вмешательства, были прогрессирование ПВР после операции и, как следствие этого, рецидив отслойки сетчатки, эпиретинальный фиброз, субретинальная пролиферация.
Сравнительный анализ течения влажной формы возрастной макулярной дегенерации в глазах с начальной катарактой и в глазах, перенесших факоэмульсификацию
Аннотация
Введение: Частое сочетание возрастной макулярной дегенерации (ВМД) с катарактой в одном глазу и теоретическое наличие риска прогрессирования дегенеративных процессов в макулярной области после оперативного удаления хрусталика ставят перед офтальмологами этические, клинические и экономические вопросы. Целью исследования стало сравнить течение влажной формы ВМД в глазах с начальной катарактой и в глазах, перенесших хирургическое лечение катаракты. Материалы и методы: 135 глаз с влажной формой ВМД, 48 глаз - основная группа - перенесли факоэмульсификацию в течение исследования, 87 глаз - контрольная группа - с начальной катарактой без показаний к хирургическому лечению. Регулярные визиты каждые 1,5 месяца в течение 2-х лет наблюдения с оценкой остроты зрения, толщины центральной сетчатки по данным оптической когерентной томографии (OKT). Инъекции ингибиторов ангиогенеза выполнялись в режиме «по необходимости». Результаты: Статистически значимой разницы между остротой зрения, центральной толщиной сетчатки, частотой интравитреальных инъекций в обоих группах на протяжении всего периода исследования нет. Выводы: Влияния факоэмульсификации на течение влажной формы ВМД не обнаружено.
Морфометрические и гемодинамические особенности течения возрастной макулярной дистрофии при сочетанной патологии: возрастная макулярная дистрофия и глаукома
Аннотация
Цель - определить характерные особенности морфометрических изменений сетчатки и показателей хориоидального кровотока у пациентов с сочетанной патологией: возрастная макулярная дистрофия (ВМД) и первичная открытоугольная глаукома (ПОУГ). Материалы и методы. Исследованы две группы пациентов: исследовательская группа 1 (ИГ1) - ВМД в сочетании с ПОУГ (113 больных), исследовательская группа 2 (И2) - ВМД без признаков нейрооптикопатии (92 пациента); средний возраст - 71,9 ± 9,3 лет. Проведено измерение толщины нейроэпителия (НЭ) и слоя ганглиозных клеток сетчатки (ГКС) в ручном режиме методом оптической когерентной томографии ОКТ (42 глаза в ИГ1, 38 глаз в ИГ2) и исследование показателей хориоидального кровотока (ХК) ультразвуковым методом (18 глаз в ИГ1, 38 глаз в ИГ2) в двух зонах: на 4 мм латеральнее (зона I) и медиальнее (зона II) диска зрительного нерва. Рассчитан индекс толщины слоя ГКС = толщина ГКС/толщина НЭ. Результаты. Установлено, что у пациентов с сочетанной патологией (ИГ1) толщина слоя ГКС в зоне I и II достоверно ниже, чем у пациентов с ВМД (ИГ2), индекс толщины слоя ГКС в исследуемых зонах достоверно снижен, в то время как у пациентов в ИГ2 данный индекс увеличивается. При исследовании ХК достоверные отличия у пациентов ИГ1 в сравнении с ИГ2 установлены в зоне I и зоне II в виде снижения показателей пиковой систолической скорости кровотока, усредненной по времени максимальной скорости кровотока, максимальной конечной диастолической скорости кровотока. Показатель индекса периферического сопротивления в ИГ1 снижен в зоне I и повышен в зоне II, в то время как в ИГ2 повышен в зоне I и снижен в зоне II. Заключение. У пациентов с сочетанной патологией ВМД и ПОУГ снижена толщина НЭ за счет истончения слоя ганглиозных клеток и формирования ишемического паттерна хориоидального кровотока в макулярной зоне и медиальнее ДЗН.
Результаты исследования нейропротекторной эффективности препарата «Семакс»
Аннотация
Цель работы: исследование эффективности и безопасности применения препарата «Семакс» 0,1 % как средства нейропротекторной терапии при ПОУГ по данным Гейдельбергской диагностики. Материалы и методы. Обследовано 36 пациентов (72 глаза) с первичной глаукомой. Первая группа была представлена пациентами с ПОУГ, получающими помимо основной гипотензивной терапии препарат «Семакс» (24 пациентов - 48 глаз). Вторую, контрольную группу составили пациенты с ПОУГ, получающие только основную офтальмогипотензивную терапию (12 человек - 24 глаза). Всем пациентам было проведено офтальмологическое исследование с помощью Гейдельбергской диагностики. Исследование в группах проводилось дважды - до начала лечения и через 1 месяц после назначения «Семакса». Результаты и обсуждение. В статье представлено исследование эффективности и безопасности применения препарата «Семакс» при первичной глаукоме по данным Гейдельбергской диагностики - сканирующей лазерной томографии, HRT-периметрии в режиме SAP III, конфокальной биомикроскопии роговицы. За период наблюдения выявлено отсутствие отрицательной динамики в структуре ДЗН и в слое суббазального нервного сплетения роговицы. Функциональное состояние зрительного анализатора по периметрическим данным также не изменялось. Нежелательных побочных реакций на препарат «Семакс» 0,1 % выявлено не было.
Опыт применения «Хилопарина» в клинической практике
Аннотация
Частота выявления синдрома «сухого глаза» среди пациентов развитых стран ежегодно растет. Это служит источником постоянного научного поиска эффективных и безопасных методов его лечения, новых офтальмологических препаратов. В связи с регистрацией в РФ «Хилопарин-комода», содержащего в своем составе гепарин, на базе нашей кафедры было проведено исследование эффективности препарата в лечении различной офтальмопатологии, протекающей на фоне ССГ.
Применение препарата «Сигницеф» для профилактики послеоперационных инфекционных осложнений
Аннотация
Цель работы: изучить эффективность и переносимость препарата «Сигницеф» при его использовании в ранние сроки после офтальмологических операций. Материалы и методы. Исследуемую группу составили 82 человека, которым проводились офтальмохирургические вмешательства. Всем пациентам проводилась стандартная схема профилактики инфекционных и воспалительных осложнений, включившая инстилляции глазных капель «Сигницеф». Оценивалось состояние переднего отрезка оперированного глаза ежедневно до выписки из стационара, а также через 7 и 14 дней после операции. Результаты. Среди пациентов исследуемой группы не отмечено ни одного случая гнойных осложнений. Объективные признаки инфекционного процесса, так же как и явления непереносимости препарата не выявлены. Выводы. Препарат «Сигницеф» обеспечил адекватную профилактику инфекционных осложнений в раннем послеоперационном периоде и продемонстрировал хорошую переносимость у пациентов исследуемой группы.
Рацемозная гемангиома радужной оболочки
Аннотация
Описаны два клинических случая рацемозной гемангиомы радужной оболочки. Мы описали клинические особенности, ангиографические и ультразвуковые характеристики опухоли. Мы считаем, что рацемозная гемангиома может приводить к развитию катаракты. Факоэмульсификация прошла без осложнений.
Синдром Гренблада-Страндберга
Аннотация
Cиндром Гренблада-Страндберга - наследственное заболевание, характеризующееся поражением эластических волокон кожи, кровеносных сосудов и глаз. Изменения на коже представлены плоскими ксантоматозными узелками желтоватого цвета. Поражение глаз характеризуется стадийностью. В первой стадии формируются ангиоидные полосы, во второй стадии образуется субретинальная неоваскулярная мембрана, что при её субфовеолярной локализации вызывает снижение зрения, третья стадия характеризуется рубцовыми изменениями.
Читайте также:
