Регуляция коронарного кровотока. Нервная регуляция сердечного кровотока
Обновлено: 24.04.2024
Регуляция коронарного кровотока. Нервная регуляция сердечного кровотока
Коронарный кровоток регулируется главным образом расширением артериол в ответ на возросшие метаболические потребности миокарда. Это значит, что, как только увеличивается сила сердечных сокращений, увеличивается и кровоток в коронарной системе. И наоборот, уменьшение активности сердца сопровождается уменьшением коронарного кровотока. Местные механизмы регуляции коронарного кровотока — такие же, как и во всех других тканях организма, особенно в скелетных мышцах.
Потребность в кислороде - главный фактор местной регуляции коронарного кровотока. Кровоток в коронарных сосудах находится в прямой пропорциональной зависимости от потребности сердечной мышцы в кислороде. Обычно сердечная мышца поглощает около 70% общего количества кислорода из протекающей артериальной крови. После этого кислорода в крови остается немного, поэтому дополнительное снабжение миокарда кислородом практически невозможно без увеличения коронарного кровотока.
К счастью, коронарный кровоток увеличивается прямо пропорционально количеству кислорода, поглощенному сердечной мышцей при усилении метаболизма.
Однако точные механизмы расширения коронарных сосудов при увеличении потребления кислорода миокардом остаются неясными. Многие исследователи предполагают, что уменьшение концентрации кислорода в тканях сердца приводит к выделению сосудорасширяющих веществ, которые вызывают расширение артериол. К веществам с выраженным сосудорасширяющим действием относят аденозин. Низкая концентрация кислорода в мышечных клетках приводит к расщеплению большого числа молекул АТФ до аденозинмонофосфата, небольшое количество которого затем расщепляется далее.
В результате в тканевую жидкость выделяется аденозин, который способствует увеличению местного коронарного кровотока. Затем большая часть аденозина реабсорбируется клетками сердца и используется ими повторно.
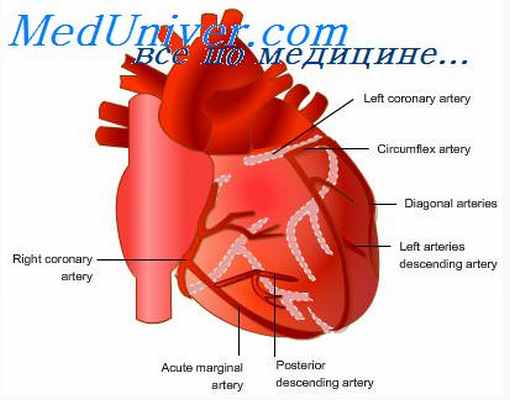
Аденозин не является единственным признанным сосудорасширяющим фактором. Другие факторы, такие как аденозинфосфаты, ионы калия, ионы водорода, углекислый газ, брадикинин, простагландины, оксид азота, также расширяют сосуды.
Существуют определенные трудности с обоснованием сосудорасширяющих гипотез. Во-первых, фармакологические агенты, которые полностью или частично блокируют сосудорасширяющее влияние аденозина, не предотвращают расширение коронарных сосудов при активации сердечных сокращений.
Во-вторых, исследования кровотока в скелетных мышцах показали, что непрерывное введение аденозина поддерживает сосудорасширяющий эффект только на протяжении 1-3 ч, в то время как сократительная активность мышц продолжает вызывать расширение сосудов даже после того, как они перестали реагировать на введение аденозина. Это подтверждает гипотезу о возможном участии многих сосудорасширяющих факторов в местной регуляции кровотока.
Нервная регуляция коронарного кровотока. Стимуляция сердечных нервов оказывает как прямое влияние на коронарный кровоток, так и непрямое. Прямое влияние развивается под действием ацетилхолина, медиатора парасимпатических (блуждающих) нервов, и норадреналина, медиатора симпатических нервов сердца. Непрямое влияние развивается вторично, за счет уменьшения или увеличения уровня метаболизма при изменении сердечной деятельности.
Непрямое влияние, которое чаще бывает противоположно прямому влиянию, играет ведущую роль в регуляции коронарного кровотока в нормальных условиях. Так, симпатическая стимуляция, приводящая к выделению большого количества адреналина и норадреналина, увеличивает частоту и силу сердечных сокращений. При этом увеличивается и уровень метаболизма в миокардиальных волокнах.
Усиление метаболизма, в свою очередь, включает механизмы местной регуляции коронарного кровотока, связанные с расширением коронарных сосудов, и коронарный кровоток увеличивается пропорционально возросшим метаболическим потребностям сердечной мышцы. И наоборот, стимуляция блуждающих нервов приводит к выделению ацетилхолина, который уменьшает частоту сердечных сокращений и несколько угнетает силу сокращений. Торможение сердечной деятельности сопровождается снижением уровня метаболизма и потребления кислорода, что приводит к сужению коронарных артерий.
Регуляция коронарного кровотока
Гипоксия — один из важнейших факторов, регулирующих коронарный кровоток. Сердечная мышца экстрагирует из притекающей крови О2 (60—70%). Потребление кислорода миокардом составляет 4—10 мл на 100 г его массы в 1 минуту, при повышении нагрузки на сердце оно возрастает, но не за счет увеличения экстракции О2, а за счет увеличения коронарного кровотока. Снижение О2 на 5% приводит к расширению коронарных сосудов. При аноксии (прекращении доставки О2 к сердцу) его сокращения постепенно ослабевают, целости сердца расширяются и через 6—10 минут наступает остановка сердца, которая вначале сопровождается биохимическими изменениями: падением содержания АТФ и креатинфосфата, накоплением лактата, который не расщепляется до СО2 и воды. После 30-минутной аноксии наступают структурные необратимые нарушения в мышце сердца: 30 минут — это предел реанимации. При удушье предел реанимации короче (8—10 мин), так как возникают необратимые изменения головного мозга.
Увеличение МОК приводит к улучшению коронарного кровотока.
Несильное раздражение симпатических нервов улучшает метаболизм сердечной мышцы и коронарный кровоток, сильное раздражение вызывает констрикторный эффект на сосудах сердца и боли в сердце.
Стимуляция парасимпатических нервов (блуждающего нерва) приводит к слабому расширению коронарных сосудов и одновременно к отрицательному инотропному эффекту, ухудшению коронарного кровотока и к смерти, особенно ночью, когда превалирует тонус блуждающего нерва.
Положительный хронотропный эффект (тахикардия) уменьшает коронарный кровоток, положительный инотропный эффект улучшает коронарный кровоток.
Адреналин и норадреналин увеличивают коронарный кровоток, ацетилхолин — уменьшает, брадикинин, простагландины — расширяют коронарные сосуды и улучшают в них кровоток. Аналогичное положительное влияние оказывает аденозин, молочная кислота, СО2, Н + ионы, Са 2+ , NO (окись азота). Передозировка ионов К + ухудшает коронарный кровоток и приводит к остановке сердца.
Фармакологическая коррекция нарушений некоторых
физиологических показателей системы кровообращения
Средства, влияющие на возбудимость, проводимость сердечной мышцы и ритм сердечных сокращений
Сердечный ритм зависит от автоматии, возбудимости и проводимости сердечной мышцы. Аритмии — нарушения ритма деятельности сердца. Они могут возникать вследствие повышения или угнетения автоматии в синоатриальном узле, а также в результате повышения автоматии или в эктопическом, или в латентном водителе ритма. Увеличение автоматии синоатриального узла называется синусовой тахикардией, уменьшение — синусовой брадикардией.
Одной из причин возникновения аритмий может быть так называемый «механизм повторного входа возбуждения» (reentry-механизм), который имеет место при пароксизмальной тахикардии, мерцании и трепетании предсердий и желудочков, экстрасистолии.
Нарушение проводимости - наиболее частая причина возникновения аритмий, включает в себя замедление или блокаду проведения импульсов, о которых говорилось выше.
Для лечения аритмий используют антиаритмические препараты, которые по механизму действия делят на пять групп.
К первой группе относят препараты с мембраностабилизирующим действием (уменьшают проницаемость клеточной мембраны и нарушают транспорт К + , Na + и Са 2+ , блокируют ацетилхолин). Эти вещества угнетают автоматию клеток синоатриального узла и эктопических водителей ритма, снижают возбудимость волокон Пуркинье и миофибрилл, уменьшают скорость проведения импульсов через атриовентрикулярный узел и волокна Пуркинье, увеличивают продолжительность ПД и абсолютной рефрактерной фазы. К этой группе препаратов относят хинидин, новокаинамид, ритмодан и др. Их принимают при мерцательной аритмии, трепетании предсердий, пароксизмальной тахикардии, частой предсердной и желудочковой экстрасистолии, желудочковой тахикардии.
Препараты К + — панангин, аспаркам, хлорид калия приводят к снижению мембранного потенциала миоцитов и уменьшению скорости проведения импульсов в миофибриллах. Их назначают при аритмиях, связанных с гипокалиемией, и при аритмиях, вызванных передозировкой дигиталиса.
Ко второй группе антиаритмических препаратов относят лидокаин, мекситил, пропафенон и др. В отличие от хинидина, эти препараты уменьшают рефрактерный период, повышают скорость проведения импульсов, не влияя на сократимость миокарда. Кроме того, они обладают местноанестезирующим действием и показаны при остром инфаркте миокарда. Их используют для лечения желудочковой экстрасистолии и профилактики фибрилляции желудочков сердца.
Антиаритмические препараты третьей группы — это блокаторы бета-адренергических рецепторов. Они уменьшают автома-тию предсердий и желудочков, снижают атриовентрикулярную и внутрижелудочковую проводимость, укорачивают время реполяризации. Их назначают при желудочковой экстрасистолии, трепетании и мерцании предсердий. К препаратам этой группы относят обзидан, оксипренолол, аптин, вискен.
Антиаритмические препараты четвертой группы обладают антиаритмическими свойствами, не влияя на мембраны за счет блокады постганглионарной симпатической передачи импульсов. Они укорачивают ПД и абсолютный рефрактерный период. Представителем этой группы является препарат кордарон. Его назначают при пароксизмальных аритмиях, синусной тахикардии, трепетании предсердий, желудочковой тахикардии и экстрасистолии.
К пятой группе антиаритмических препаратов относят антагонисты кальция, например верапамил (изоптин, финоптин). Он тормозит трансмембранный ток Са 2+ внутри сердечной клетки, уменьшает спонтанную активность синоатриального узла.
Регуляция коронарного кровотока. Нервная регуляция сердечного кровотока
Регуляция коронарного кровотока. Нервная регуляция сердечного кровотока
Уровень метаболизма в миокарде является ведущим фактором регуляции коронарного кровотока. Коронарный кровоток регулируется главным образом расширением артериол в ответ на возросшие метаболические потребности миокарда. Это значит, что, как только увеличивается сила сердечных сокращений, увеличивается и кровоток в коронарной системе. И наоборот, уменьшение активности сердца сопровождается уменьшением коронарного кровотока. Местные механизмы регуляции коронарного кровотока — такие же, как и во всех других тканях организма, особенно в скелетных мышцах.
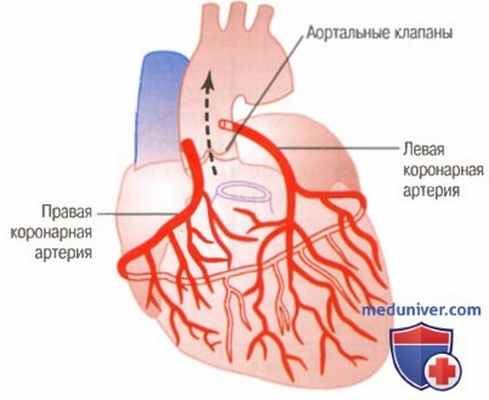
Коронарные артерии
а) Потребность в кислороде - главный фактор местной регуляции коронарного кровотока. Кровоток в коронарных сосудах находится в прямой пропорциональной зависимости от потребности сердечной мышцы в кислороде. Обычно сердечная мышца поглощает около 70% общего количества кислорода из протекающей артериальной крови. После этого кислорода в крови остается немного, поэтому дополнительное снабжение миокарда кислородом практически невозможно без увеличения коронарного кровотока.
К счастью, коронарный кровоток увеличивается прямо пропорционально количеству кислорода, поглощенному сердечной мышцей при усилении метаболизма.
Однако точные механизмы расширения коронарных сосудов при увеличении потребления кислорода миокардом остаются неясными. Многие исследователи предполагают, что уменьшение концентрации кислорода в тканях сердца приводит к выделению сосудорасширяющих веществ, которые вызывают расширение артериол. К веществам с выраженным сосудорасширяющим действием относят аденозин. Низкая концентрация кислорода в мышечных клетках приводит к расщеплению большого числа молекул АТФ до аденозинмонофосфата, небольшое количество которого затем расщепляется далее.
В результате в тканевую жидкость выделяется аденозин, который способствует увеличению местного коронарного кровотока. Затем большая часть аденозина реабсорбируется клетками сердца и используется ими повторно.
Аденозин не является единственным признанным сосудорасширяющим фактором. Другие факторы, такие как аденозинфосфаты, ионы калия, ионы водорода, углекислый газ, брадикинин, простагландины, оксид азота, также расширяют сосуды.
Существуют определенные трудности с обоснованием сосудорасширяющих гипотез. Во-первых, фармакологические агенты, которые полностью или частично блокируют сосудорасширяющее влияние аденозина, не предотвращают расширение коронарных сосудов при активации сердечных сокращений.
Во-вторых, исследования кровотока в скелетных мышцах показали, что непрерывное введение аденозина поддерживает сосудорасширяющий эффект только на протяжении 1-3 ч, в то время как сократительная активность мышц продолжает вызывать расширение сосудов даже после того, как они перестали реагировать на введение аденозина. Это подтверждает гипотезу о возможном участии многих сосудорасширяющих факторов в местной регуляции кровотока.
б) Нервная регуляция коронарного кровотока. Стимуляция сердечных нервов оказывает как прямое влияние на коронарный кровоток, так и непрямое. Прямое влияние развивается под действием ацетилхолина, медиатора парасимпатических (блуждающих) нервов, и норадреналина, медиатора симпатических нервов сердца. Непрямое влияние развивается вторично, за счет уменьшения или увеличения уровня метаболизма при изменении сердечной деятельности.
Непрямое влияние, которое чаще бывает противоположно прямому влиянию, играет ведущую роль в регуляции коронарного кровотока в нормальных условиях. Так, симпатическая стимуляция, приводящая к выделению большого количества адреналина и норадреналина, увеличивает частоту и силу сердечных сокращений. При этом увеличивается и уровень метаболизма в миокардиальных волокнах.
Усиление метаболизма, в свою очередь, включает механизмы местной регуляции коронарного кровотока, связанные с расширением коронарных сосудов, и коронарный кровоток увеличивается пропорционально возросшим метаболическим потребностям сердечной мышцы. И наоборот, стимуляция блуждающих нервов приводит к выделению ацетилхолина, который уменьшает частоту сердечных сокращений и несколько угнетает силу сокращений. Торможение сердечной деятельности сопровождается снижением уровня метаболизма и потребления кислорода, что приводит к сужению коронарных артерий.
Учебное видео кровоснабжения сердца (анатомии артерий и вен)
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Регуляция коронарного кровотока.
Потребность миокарда в кислороде является главным фактором регуляции коронарного кровотока. Повышение силы сердечных сокращений сопровождается увеличением кровоснабжения миокарда и, наоборот, уменьшение работы сердца приводит к уменьшению кровотока по венечным сосудам. При максимальном расширении венечных артерий сердца кровоснабжение миокарда может увеличиться в 6 раз.
Регуляция коронарного кровотока осуществляют три универсальных механизма — миогенный, нейрогенный и гуморальный.
Миогеннаярегуляция. Тонус венечных сосудов сердца опосредуется напряжением гладкомышечных клеток сосудистой стенки и зависит от степени ее растяжения. При снижении давления в венечных артериях их стенки расслабляются, а просвет увеличивается.
Нейрогенная регуляция. Осуществляется посредством выделения из нервных окончаний медиаторов — норадреналина, ацетилхолина, нейропептидов и других веществ, которые действуют на соответствующие рецепторы (а, |3 и др.) гладкомышечных клеток и эндотелия. В результате происходит расширение (вазодилатация) или сужение (вазоконстрикция) сосудов сердца.
Гуморальная регуляция. Венечные сосуды сердца отвечают повышением или снижением тонуса гладкомышечных клеток на действие биологически активных веществ, поступающих с кровью и образующихся в сосудистой стенке. Расширение венечных сосудов происходит главным образом за счет действия оксида азота, синтезируемого эндотелием, а сужение — под действие эндотелиальных факторов (эндотелии), а также вазоконстрикторов, которые продуцируют тромбоциты (тромбоксан Л2) и ренин-ангиотензин-альдо- стероновая система (ангиотензин II).
Основным механизмом увеличения кровотока по венечным сосудам при физической нагрузке является усиление тонуса симпатического отдела вегетативной нервной системы и прямая нейрогенная стимуляция (3-адренорецепторов венечных артерий, приводящая к их расширению. При тяжелой физической нагрузке коронарный кровоток может возрастать в 3—4 раза.
Иннервация сердца. Сердце имеет парасимпатическую (холинергическую) и симпатическую (адренергическую) иннервацию. Внутри сердца существует собственная (автономная) нервная сеть. Она включает афферентные нейроны, дендриты которых имеют рецепторы растяжения на кардиомиоцитах и венечных сосудах, а также эфферентные нейроны, аксоны которых подходят к кардиомиоцитам. Вблизи водителей ритма сердца (синоатриального и атриовентрикулярного) расположены внутрисердечные нервные узлы. С ними контактируют эфферентные волокна парасимпатических и симпатических нервов, образующие внутрисердечные нервные сплетения.
Парасимпатические волокна являются аксонами нейронов ядер, расположенных в продолговатом мозге. Они проходят в составе правого и левого блуждающих нервов. Волокна правого блуждающего нерва иннервируют преимущественно правое предсердие и синоатриальный узел (главный водитель ритма сердца), а левого — главным образом атриовентрикулярный узел (водитель ритма второго порядка). В миокарде преганглионарные парасимпатические волокна образуют синапсы с внутрисердечными нейронами. Наибольшее влияние центральные холинергические стимулы оказывают на предсердия, в меньшей степени они действуют на желудочки сердца.
Симпатические влияния к сердцу поступают по нервным волокнам, которые являются аксонами нейронов боковых рогов верхних грудных сегментов спинного мозга. Они прерываются в шейных симпатических ганглиях. Постганглионарные симпатические волокна подходят ко всем отделам сердца в составе нескольких нервов. Плотность симпатических нервных волокон в правом желудочке сердца больше, чем в левом. Синоатриальный узел иннервируется преимущественно правым симпатическим нервом, а атриовентрикулярный водитель ритма — преимущественно левым симпатическим нервом. Сердце в различных отделах имеет рецепторы, которые генерируют афферентные сигналы, поступающие в сосудодвигательный центр головного мозга. Из сердца в ЦНС они проходят в составе волокон парасимпатических и симпатических нервов.
Строение миокарда. Функциональным элементом миокарда является мышечное волокно. Мышечное волокно образованно цепочкой кардиомиоцитов, которые соединены вставочными дисками и заключены в общую сарколемму. Вставочные диски прочно удерживают мембраны клеток, образуя щелевые контакты (электрический синапс) — нексусы (рис. 5.3.8). Кардиомиоциты контактируют друг с другом, не препятствуя обмену ионов через щелевые контакты и распространению потенциалов действия в сердечной мышце.
![Схема электрической (А) и химической (Б) синаптических передач [14]](/pimg1/regulyatsiya-koronarnogo-krovotoka-863B.png)
Рис. 5.3.8. Схема электрической (А) и химической (Б) синаптических передач [14]
В электрическом синапсе скорость передачи сигнала в 2—3 раза больше, чем при химической (медиаторной) синаптической передаче. Таким образом, сердечная мышца представляет собой сеть кардиомиоцитов (синцитий), которые тесно контактируют друг с другом. При возбуждении даже одного кардиомиоцита происходит мгновенное распространение потенциала действия на клетки миокарда в целом (рис. 5.3.9. Микроструктура миокардаС^Ь).
Основные свойства миокарда. Миокард обладает физическими и электрофизиологическими свойствами. Сердечная мышца способна под действием силы увеличивать длину без нарушения своей структуры и полностью восстанавливать исходный размер после прекращения деформирующего воздействия. В процессе сокращения миокард развивает силу и совершает работу по перемещению крови в системе циркуляции. Основными электрофизиологическими свойствами миокарда являются возбудимость, автоматизм, проводимость и сократимость.
Возбудимость. Под возбудимостью миокарда понимают способность кардиомиоцитов мгновенно отвечать на пороговый раздражитель (потенциала действия — ПД) возбуждением — сокращением.
Потенциал покоя. На мембранах сократительных (типичных) кардиомиоцитов в покое поддерживается электрический потенциал покоя (ПП), равный —90 мВ. Потенциал покоя поддерживается вследствие более быстрого, по сравнению с высокомолекулярными анионами, выхода ионов калия из цитоплазмы в интерстиций. Величина ПП целиком зависит от скорости (пассивного) транспорта ионов калия через мембрану по градиенту концентрации. Вклад активного (потенциалзависимого) транспорта ионов калия в формировании ПП составляет менее 10%. Поэтому даже при полной блокаде энергозависимых калиевых каналов величина потенциала покоя мембраны кардиомиоцитов практически не изменяется.
Потенциал действия. При возбуждении сократительные кардиомиоциты генерируют потенциал действия (ПД) (рис. 5.3.10). В формировании ПД участвуют только потенциалзависимые ионные каналы. В ПД выделяют две фазы — деполяризацию и реполяризацию мембраны. Крутой фронт кривой деполяризации (0) обусловлен открытием быстрых натриевых каналов и интенсивным поступлением Na + из внеклеточной жидкости в клетку. При достижении мембранного потенциала (МП) величины —40 мВ в процесс деполяризации мембраны включаются медленные натрий-кальциевые каналы. К быстрому натриевому току присоединяется транспорт ионов кальция, а также ионов хлора.

Рис. 5.3.10. Фазы потенциала действия клеток с «быстрым» [а) и «медленным» (б) ответом (цит. по Г.Е. Ротенбергу, А.В. Струтынскому, 2003)
Когда мембранный потенциал достигает величины 15—20 мВ, быстрые натриевые каналы закрываются, а прирост амплитуды МП прекращается. Вместе с тем поступление ионов кальция и натрия в клетку по медленным каналам в клетку не прекращается.
Автоматизм. Под автоматизмом понимают способность миокарда ритмично сокращаться под влиянием потенциалов действия (ПД), возникающих в самом сердце вне связи с внешними стимулами. Источником автоматизма сердечной мышцы являются атипичные волокна миокарда, мембраны которых во время диастолы самопроизвольно (спонтанно) деполяризуются до критического уровня и генерируют ПД (см. рис. 5.3.10, б).
В атипичных клетках, в отличие от сократительных кардиомиоцитов, устойчивой поляризации мембран не существует, а «потенциал покоя» не превышает —60 мВ. При достижении этой величины вследствие спонтанного поступления ионов натрия и кальция через мембрану в клетку МП сразу же смещается к пороговому уровню (0). Порогом деполяризации для ПД является величина —40 мВ. Амплитуда и скорость ПД в фазе деполяризации (см. рис. 5.3.10, б, 1) целиком определяется работой медленных натрий-кальциевых каналов, поскольку при напряжении на мембране менее —55 мВ быстрые натриевые каналы инактивированы. Фаза реполяризации определяется выключением натрий-кальциевых каналов и более длительным выходом ионов калия из клетки (см. рис. 5.3.10, б, 2). Это приводит к смещению уровня мембранного потенциала ниже порогового значения (36) и гиперполяризации мембраны (до —60 мВ).
Регуляция коронарного кровотока

при изменении системного артериального давления в пределах 70-160 мм рт. ст. Так, при повышении давления в коронарных сосудах наступает сокращение гладких мышц, при снижении - гладкие мышцы стенки сосуда расслабляются.
Нервная регуляция. В начале исследований коронарного кровотока довести его нервную регуляцию было довольно трудно. Во-первых, потому что долгое время не могли выявить наличие нервных окончаний на коронарных сосудах. Во-вторых, потому что под влиянием нервной стимуляции изменяется работа сердца, которая может влиять на функции сосудов. Однако установлено наличие адренергических и холинергических окончаний, стабилизация работы сердца позволили подтвердить прямое влияние симпатической и парасимпатической нервных систем на коронарные сосуды.
Стимуляция симпатической нервной системы (подраз ния звездчатого шейного ганглия) и парасимпатической нервной системы (раздражение блуждающего нерва) вызывает расширение коронарных сосудов, увеличение коронарного кровотока.
Рефлекторные влияния с коронарных сосудов. Koронарни сосуды очень много обеспечены нервами в виде скоплений, древовидных разветвлений диффузных окончаний, высокочувствительных к изменениям давления крови. Так, при повышении давления в левой артерии, особенно в области ее бифуркации, развивается системная депрессорных реакция и брадикардия, что блокируются вапотомиею. При снижении коронарного давления наблюдаются Прессорный реакция и тахикардия, которая связана с повышением активности симпатической нервной системы. Эти данные позволяют сделать вывод, что 8 коронарных сосудах заложены механорецелторы, которые реагируют на изменение давления крови.
В коронарных сосудах находятся и хеморецепторы, реагирующие на введение химических веществ, например, вератрин, что приводит к брадикардии и системной гипотензии. При ограничении коронарного кровотока или пережимание коронарного сосуда развиваются изменения ЭКГ и значительная болевая реакция, связанная с резким возбуждением симпатической нервной системы и ее афферентных волокон. Пересечение их значительно ослабляет или устраняет болевой синдром.
Гуморальная регуляция. Медиатор парасимпатической нервной системы - ацетилхолин приводит к выразительной дилатации коронарных сосудов, увеличение коронарного кровотока. Его эффект тормозится блокиратором М-холинорецепторов - атропином.
Медиатор симпатической нервной системы - норадреналин - вызывает также расширение коронарных сосудов, повышение коронарного кровообращения, и это влияние связано с β-рецепторами коронарных сосудов. Блокада их β-адренорецепторов - Индерал - предупреждает дилататорний эффект и увеличение кровотока.
Известно, что в коронарных сосудах находятся α- и β-адренорецепторы, то есть две точки приложения катехоламинов. В начале коронарных сосудов размещены α-адренорецепторы, их количество невелико. β-адренорецепторы находятся в дистальном отделе сосудов малого диаметра в большом количестве, поэтому результирующей реакцией является дилатация. Сдавление коронарных сосудов под влиянием катехоламинов наблюдается на фоне блокады β-адренорецепторов, когда они только взаимодействуют с а-адренорецепторами. Блокада их α-адренорецепторов - регитином предупреждает констрикторний эффект. Подобный эффект - сужение коронарных сосудов под влиянием симпато- надпочечниковой системы - наблюдается довольно часто у старых животных, у которых выявлено уменьшение количества β-адренорецепторов в сосудах сердца.
Вызывают расширение коронарных сосудов гормоны инсулин, тироксин; сужение - адреналин, вазопрессин, ангиотензин и др.
Метаболическая регуляция. Тяжелая физическая работа сопровождается резким ростом сердечного выброса (в 5-8 раз) и коронарного кровотока (в 4,5 раза), что приводит к резкому повышению метаболизма в сердце - поглощение кислорода увеличивается в три раза (от 30 до 90 мл / мин). Недостаточность O2 вызывает "деградации" АТФ на АДФ, затем на АМФ и аденозин (блокирует Са 2+ - каналы), который проникает через мембраны кардиомиоцитов в межклеточное пространство и повышает местный коронарный кровоток. Такой же эффект, кроме аденозина, вызывают СО2, ионы Н + и К +, оксид азота, брадикинин и простагландины, гистамин и молочная кислота.
Основными факторами, влияющими на величину коронарного кровотока, являются физические - величина давления крови в аорте и частота сокращений желудочков, метаболические - вазодилатация возникает благодаря метаболита - аденозина. Нервная регуляция тонуса коронарных сосудов имеет меньшее значение.
Читайте также:
