Трехмерная эхокардиография при врожденных пороках сердца
Обновлено: 18.04.2024
Врожденные пороки сердца (пороки сердца) – аномальное строение камер сердца, крупных сосудов или клапанов (нередки и сочетания) вследствие генетической предрасположенности, нарушений внутриутробного развития, инфекционных, аутоиммунных, метаболических и других заболеваний, травм, полученных матерью во время беременности.
Поражения клапанов могут быть врожденными (из-за нарушений внутриутробного развития) и приобретенными, то есть возникающими в течение жизни под воздействием заболеваний, инфекций или травм. В большинстве случаев, сложные врожденные пороки требуют хирургической коррекции как у детей, так и взрослых.
Какие существуют врожденные пороки сердца
Причина возникновения порока сердца
Какие бывают последствия
Если деффект большой, то со временем возникает сердечная недостаточность.
Диагностика и лечение порока сердца
Своевременно распознать и устранить деффект могут кардиохирурги. В большинстве случаев, закрывают деффект рентгенохирурги с использованием катетерной техники, не прибегая к разрезу.
- Деффект может появиться между желудочками сердца - деффект межжелудочковой перегородки.
- Нередко деффекты сочетаются с аномалиями клпанного аппарата серодца или крупных сосудов.
Клапанный аппарат сердца состоит из четырех клапанов: митрального (двустворчатого), трикуспидального (трехстворчатого), аортального и клапана легочной артерии. От слаженной и правильной работы этих структур зависит работа сердца.
Существует два основных типа поражения клапана: недостаточность и стеноз.
В грудном сегменте аорта прикрепляется к задней стенке, ближе к позвоночнику. В этом месте порой аорта значително сужена, внутренние органы не получают достаточного количества артериальной крови. Раньше это состояние, называемое коарктацией аорты, устранялось только хирургическим путем. Но сегодня, в большинстве случаев, сужение при корактации аорты устраняют баллонной диллятацией и установкой каркаса-стента. Следует подчеркнуть, что если стеноз клапана является изолированным поражением, то это часто устранается баллонным расширением, минимально травматичным путем.
Как проявляются заболевания клапанов сердца
Чаще всего жалобы пациентов неспецифичны: одышка, учащенный пульс, аритмия, быстрая утомляемость, синюшность, головокружение.
Выраженность и характер симптомов зависят от расположения пораженного клапана. При пороках клапанов левой половины сердца (митральный и аортальный) в первую очередь страдают легкие, т.к. в их сосудах застаивается кровь, что проявляется одышкой. Так же возникают признаки недостаточного кровоснабжения всех органов и систем, в первую очередь, головного мозга и самого сердца. Возникает головокружение, обмороки, стенокардия. При нарушении работы клапанов правой половины сердца (трикуспидальный и клапан легочной артерии), происходит застой крови в сосудах большого круга кровообращения, т.е. страдают все органы, кроме легких. Развиваются отеки голеней и стоп, асцит (жидкость в брюшной полости), увеличение печени и т.д (УВЕЛИЧИВАЕТСЯ ПЕЧЕНЬ И Т.Д.).
Пороки клапанов сердца опасны своими осложнениями и влиянием на организм, поэтому главная профилактика патологических состояний – это регулярные обследования и лечение заболеваний, ведущих к формированию клапанных дефектов.
Объем обследования определяет врач. В перечень возможных диагностических процедур входят:
- ЭКГ
- Холтеровское мониторирование ЭКГ
- Эхокардиография
- Чреспищеводная эхокардография
- 3D-эхокардиография
- 3D допплеровское цветовое изображение
- МРТ
- Катетеризация сердца
Почему стоит пройти обследование в ФНКЦ ФМБА
Специалисты кардиохирургического отделения ФНКЦ ФМБА успешно применяют передовые методы лечения заболеваний клапанов сердца у взрослых (старше 18 лет). В нашей клинике проводятся уникальные операции с минимальной инвазией, а также качественная диагностика различных форм аритмии, ишемической болезни сердца и других сердечно-сосудистых заболеваний.
Трехмерная эхокардиография при врожденных пороках сердца
Трехмерная эхокардиография при врожденных пороках сердца
Преимущество трехмерной ЭхоКГ заключается в возможности представить исследователю пространственные взаиморасположения и связь с соседними структурами патологических объектов в простом и сравнительно понятном виде. По этой причине уже на ранней стадии развития трехмерной ЭхоКГ ее существенной областью применения как раз считалась визуализация сложных врожденных пороков.
Однако до сих пор не доказано, действительно ли такое облегченное и улучшенное описание сложных пространственных взаимосвязей влияет на результат оперативного лечения пациента или же является лишь более простым способом предоперационного изложения ситуации кардиохирургу.
а) Количественный анализ. Исследования последних лет демонстрируют клинически значимые преимущества этой неинвазивной техники и при количественном анализе врожденных пороков сердца - так, например, при точной оценке желудочковой функции у пациентов с одножелудочковым сердцем, что ранее в достаточно воспроизводимой форме было возможно лишь с помощью инвазивных или облучающих методик, таких как ангиография или радионуклидная вентрикулография.
б) Дефект межпредсердной перегородки типа ostium secundum. Одно из преимуществ трехмерной ЭхоКГ становится видно при оценке гораздо менее сложного врожденного порока сердца - ДМПП типа ostium secundum. Для планирования инвазивного вмешательства по закрытию ДМПП решающее значение имеют точное определение размеров и оценка расположенных вокруг дефекта остатков перегородки - особенно в проблемной нижней зоне, что при использовании общепринятой методики сечений в некоторых случаях довольно затруднительно.
Трехмерная визуализация позволяет получить (невозможное в традиционной ЭхоКГ) фронтальное изображение дефекта со всем его окружением. Таким способом, кроме непосредственного измерения дефекта, можно обнаружить и количественно оценить изменение его размеров во время сердечного цикла с выявлением конечно-систолического максимума и конечно-диастолического минимума.
Трехмерно реконструированные перспективы у пациента с врожденной корригированной транспозицией, большим дефектом межжелудочковой перегородки (VSD) и рудиментарным правым желудочком (RV).
На кадре слева показано продольное сечение через левый желудочек (LV), из которого исходит отчетливо расширенная легочная артерия (РА); кроме того, здесь же фронтальный вид на расположенный в глубине VSD.
При реконструкции сечения по зеленой оси получается кадр в центре, на котором хорошо видно параллельное отхождение РА и восходящей части аорты (АоА).
Кадр справа представляет сечение по желтой оси. На этом сечении видны оба желудочка, больший левый и рудиментарный правый. Изображение ДМПП типа ostium secundum. На левом кадре приведен вид со стороны левого предсердия.
Можно найти устья легочных вен (PV) и измерить расстояние от них до дефекта. Пунктирная линия показывает внешние анатомические границы межпредсердной перегородки, определяющие ширину септального края, что имеет решающее значение для подготовки хирургического вмешательства.
Два изображения справа показывают вид со стороны правого предсердия на хорошо видимый центральный дефект. На трехмерном изображении можно измерить пространственное расстояние до верхней полой вены (VCS) и до трехстворчатого клапана (ТК). Также отчетливо видно различие между величиной дефекта в систолу (середина, диаметр больше) и в диастолу (справа, диаметр меньше).
Трехмерная эхокардиография при врожденных пороках сердца
Ультразвуковое исследование сердца или эхокардиография (ЭхоКГ)
Эхокардиография (ЭхоКГ) – метод ультразвуковой диагностики, направленный на исследование морфологических и функциональных изменений сердца и его клапанного аппарата. ЭхоКГ – наиболее используемый визуализирующий метод диагностики сердечно-сосудистых заболеваний (ССЗ).
2D- и 3D-ЭхоКГ позволяет в режиме реального времени детально исследовать морфологию сердца с очень высоким пространственным (‹1 мм) и временным (>100 кадров/с) разрешением. Кроме того, допплерография и методика отслеживания дифракционных пятен (“speckle tracking”) предоставляют возможность определения скорости кровотока и движения миокарда в любой точке сердца, позволяя оценивать кровоток при клапанных (стенозе или регургитации) и врожденных пороках, а также движение и деформацию миокарда, что способствует выявлению функциональных нарушений, например при ишемии или кардиомиопатиях.
ЭхоКГ неинвазивна и не связана с воздействием ионизирующего излучения; эхокардиографическое оборудование портативно и дает возможность выполнения исследования у постели больного. По особым показаниям выполняют “полуинвазивное” (чреспищеводное) или инвазивное (внутрисосудистое) УЗИ. Последние достижения в ЭхоКГ – ее использование при нагрузочных пробах, особенно для выявления ишемии миокарда, и при контрастировании правых и левых камер сердца. Благодаря повсеместной доступности, отсутствию вредного воздействия, относительно низкой стоимости в сочетании с высокой диагностической ценностью ЭхоКГ стоит первой в ряду визуализирующих методик в кардиологии и показана практически при любом ССЗ.
ЭхоКГ (эхокардиография) трансторакальная
В повседневной практике ЭхоКГ выполняют трансторакально. Исследователь сидит справа или слева от пациента, одной рукой держит датчик, другой – управляет настройками прибора, сосредоточиваясь при этом на изображении на экране монитора. Место локации и положение датчика определяют получаемое изображение. Качество получаемых ЭхоКГ-изображений зависит как от квалификации исследователя, так и от особенностей пациента. Трудно проводить исследование у больных с эмфиземой легких (например, страдающих ХОБЛ или находящихся на искусственной вентиляции легких), деформацией грудной клетки или выраженным ожирением, хотя практически у любого пациента можно найти, по крайней мере, один доступ с приемлемой визуализацией.
Продолжительность исследования зависит от трудности получения изображений и имеющейся патологии. Последние Европейские рекомендации отводят в среднем 30 мин на одно исследование, включая написание заключения. Каждое ЭхоКГ сохраняется на цифровом носителе (предпочтительно) или видеопленке, на которых должны быть представлены все полученные сечения.
Допплерэхокардиография
Помимо отображения морфологии структур сердца, ЭхоКГ дает информацию об их движении и производных параметрах. Допплеровское исследование скорости кровотока дает чрезвычайно важную информацию о клапанных и врожденных пороках, наполнении ЛЖ. В основе допплеровских измерений лежит расчет скорости движения объекта по изменению частоты отраженного сигнала. Обычно допплеровский сдвиг частот находится в пределах воспринимаемого человеческим ухом диапазона и может быть воспроизведен эхокардиографом в виде звука.
1. Импульсный допплеровский режим позволяет оценить кровоток в определенной области посредством размещения в ней контрольного объема.
2. Постоянноволновой допплеровский режим дает возможность определить любую величину скорости кровотока, однако он не позволяет точно установить место на протяжении ультразвукового пучка, в котором измеряется максимальная скорость. Таким образом, постоянноволновой и импульсный допплеровские режимы дополняют друг друга: первый дает возможность обнаружения очень высоких скоростей без уточнения их локализации; с помощью последнего, напротив, возможно установление локализации скоростей, но нельзя оценивать высокоскоростные потоки.
3. Цветное допплеровское картирование – режим, при котором скорости кровотока кодируются различными цветами, а цветовая карта накладывается на 2D- или 3D-изображение. Обычно красным цветом кодируют скорости кровотока, направленного к датчику, синим – от датчика. Определение скоростей, которые затем кодируются определенным цветом, происходит путем множественных измерений в режиме, напоминающем импульсную допплерографию, с использованием метода упрощенного анализа, называемого автокорреляцией.
Допплеровский анализ высокоамплитудных низкоскоростных ультразвуковых импульсов от тканей сердца носит название тканевой допплерографии. Ее применяют главным образом для оценки функций миокарда. Измерение продольных (от верхушки к основанию) скоростей базальных сегментов ЛЖ дает информацию о его общей систолической и диастолической функции. Кроме того, по пространственному градиенту скоростей можно рассчитать скорость региональной деформации (“strain rate”), измеряемую в с-1, или герцах, а интегрирование скорости деформации по времени позволяет вычислять собственно деформацию (“strain”), измеряемую в процентах. Деформация представляет собой укорочение и удлинение миокарда в продольном направлении в верхушечных сечениях, а также утолщение или истончение по короткой оси в парастернальных сечениях. Преимущество оценки деформации – ее истинно локальный характер, в то время как на скорость движения миокарда всегда оказывает влияние движение соседних сегментов (“tethering” или “привязывание”) и всего сердца в целом. Недавно появилась возможность оценки деформации с помощью методики отслеживания дифракционных пятен, которая не является допплеровской и, следовательно, не зависит от угла сканирования. Этот метод позволяет измерять региональные тканевые скорости, деформацию и скорость деформации в любых направлениях. Тканевые скорости, деформация и скорость деформации могут быть представлены на экране в 2D-цветном режиме и в графическом виде (изменение скорости во времени).
Трехмерная эхокардиография (3D-ЭхоКГ) трансторакальная
В настоящее время существует три варианта получения трехмерного изображения сердца: «живая» трехмерная ЭхоКГ (Live 3D) – в объеме усеченного конуса с углом сектора 30º, трехмерная ЭхоКГ в полном объеме (Full-volume) – с более широким углом лоцирования (пирамида 80º) и трехмерное цветное картирование (3D Color).
При обычном эхокардиографическом исследовании со стандартным обеспечением не представляется возможным получить множество параллельных срезов желудочка по короткой оси, и свое реальное воплощение эта идея получила только с появлением метода трехмерного моделирования ультразвукового изображения. Главное преимущество метода трехмерной реконструкции – возможность отказа от геометрических допущений и измерение объемов желудочка с учетом его конкретной формы.
Трехмерное изображение позволяет не только измерить объемы и фракцию выброса желудочка с измененной геометрией, но также определить локализацию и измерить объем аневризмы левого желудочка, что имеет несомненное значение в кардиохирургии.
Трехмерная эхокардиография в масштабе реального времени и контрастные вещества нового поколения также дают возможность оценки миокардиальной перфузии. Ультразвуковая визуализация дефектов накопления контрастного вещества в миокарде позволяет установить локализацию и распространенность зон ишемии или рубцовых изменений, а также установить взаимосвязь этих зон с поражением соответствующих коронарных артерий.
Практически значимое применение трехмерная эхокардиография находит в получении дополнительной информации о таких врожденных пороках, как: дефекты межпредсердной перегородки (ДМПП), дефекты межжелудочковой перегородки (ДМЖП), аномалии атриовентрикулярных и полулунных клапанов, аномалии выносящего тракта желудочков.
Источник:
Машина Т.В. В кн.: Бокерия Л.А., Голухова Е.З. (ред.) Клиническая кардиология: диагностика и лечение. М.: Издательство НЦССХ им. А.Н. Бакулева; 2011
Как устанавливается диагноз? Методы детской диагностики
Опытному врачу внешний вид ребенка и подробные сведения от вас, ваши наблюдения и мысли о его состоянии, результат осмотра, выслушивание сердца уже многое скажут. На этом этапе поставить точный диагноз трудно, чаще – невозможно, но заподозрить «есть порок сердца – или нет» вполне реально, и следующим этапом обследования должны стать уже специальные методы детской кардиологии. Их можно разделить на две категории: неинвазивные и инвазивные.
Первые – это способы, при которых ребенок изучается как бы «снаружи». Ему не делают никаких уколов, не усыпляют. Его надо только успокоить, чтобы он – не испугался и не плакал. А это ваша, совместная с врачом, задача. Успокойтесь сами и успокойте его. Вам предстоит период тревожного терпения, которого, к сожалению, избежать нельзя.
К неинвазивным методам относятся электрокардиография, рентгенологическое обследование, ультразвуковое исследование. Каждый из них необходим, и каждый - дополняет другой.
Скажем сразу, что не всегда, не при всех пороках и далеко не всем детям необходим весь перечисленный набор диагностических процедур. Часто можно установить диагноз на основании некоторых из них. Но информация должна быть полной и исчерпывающей прежде, чем будет поставлен вопрос об операции.
Электрокардиография (ЭКГ)– наиболее традиционный и «старый» метод обследования. Он очень информативен, но недостаточен для точного диагноза: ЭКГ дает возможность сказать, какие отделы сердца перегружены и насколько, точно определяет нарушения ритма сердца и их происхождение, но почему это происходит – не скажет.
Рентгеноскопия и рентгенография также традиционный метод исследования. Информация тоже обширная, но тоже – косвенная. Зато это метод, который дает возможность видеть и оценить не только размеры сердца, его камер, положение его в грудной клетке, но и состояние сосудов легких (переполнены они или обеднены, увеличены или нет). Обследование проводят в совершенно темном кабинете, где ребенку может стать очень страшно, поэтому, если речь идет не о совсем маленьком, его надо хорошо подготовить: успокоить, постараться объяснить, что его ожидает и о чем его будут просить, а главное, убедить, что ему не будет больно. Это задача и медицинского работника, и ваша. К сожалению, широко бытует мнение, что исследование опасно из-за «облучения».На современном оборудовании дозы радиации, которые получает ребенок, настолько малы, что никогда и никак не могут сказаться на его развитии и последующей жизни. А утверждения, что это не так – ложны и могут исходить только от людей, совершенно ничего не понимающих ни в физике, ни в медицине.
Эхокадиография (УЗИ) – сегодня самый важный и информативный метод исследования, который позволяет поставить точный диагноз и не только дополнить, но и, подчас, заменить другие, более травматичные для ребенка методы исследования. Эхокардиография стала отдельной наукой, и она может дать огромный поток нужной, необходимой информации – важно лишь правильно разбираться в этом потоке.
Благодаря УЗИ впервые в истории появилась прямая возможность увидеть сердце ребенка до родов, и современные методы позволяют диагностировать врожденный порок сердца при беременности и «возрасте плода» всего несколько недель. Прежде всего заметны (и это особенно важно) пороки, при которых строение сердца резко нарушено, т.е. очень тяжелые и сложные для исправления в последующем. И тогда семья может быть поставлена перед выбором – оставить или прервать беременность.
У родившегося ребенка УЗИ позволяет определить очень много: наличие и размер дефектов, сужение или расширение отделов сердца и его клапанов, т.е. наличие или отсутствие структурных изменений. Но, кроме того, оно дает возможность определить давление в полостях сердца, разницу давления между камерами, установить величину и направление сброса крови, если он есть, толщину стенок предсердий и желудочков. Словом – узнатьвсе или почти все. УЗИ дает возможность наблюдать за течением порока в динамике – т.е. видеть, что происходит с сердцем, как оно реагирует на случившиеся, в каком направлении идут эти изменения – к улучшению или, напротив, к ухудшению. Иными словами, оно может дать сигнал – надо ли активно вмешиваться, чтобы помочь, и когда, чтобы не было слишком поздно. И, если учесть, что метод этот - неинвазивен, абсолютно безопасен и может быть повторен неоднократно и безболезненно – то понятно, что он стал основой сегодняшней диагностики. Эхокардиографом должен быть оборудован каждый кардиологический кабинет в каждой поликлинике. И, если этого нет, надо идти туда, где – есть.
Правильный диагноз – это и есть квинтэссенция будущего результата лечения. Чем тяжелее болезнь, тем более значима диагностика. Сегодняшние возможности диагностики нередко позволяют до операции увидеть больше, чем внутри операционного поля. Именно поэтому стало возможным развитие альтернативных методов лечения, каковыми являются миниинвазивные пособия, эндоваскулярная хирургия и другое. Врачи много бьются над тем, чтобы свести воедино данные разных методов исследования и получить полное представление о заболевании сердца. Огромное значение при диагностике сложных врожденных пороков сердца, а также различных сочетанных патологий, которые, к сожалению, не редки, приобрели в последние годы такие методы как компьютерная томография, ядерно-магнитный резонанс с трехмерной реконструкцией изображения, радионуклидные методы исследования – позитронно-эмиссионная томография, сцинтиграфия миокарда и легких. Все эти методы дают врачам возможность уже при неинвазивном исследовании рассмотреть полностью межпредсердную или межжелудочковую перегородки, папиллярные мышцы желудочков, как выглядят створки клапанов в ту или иную фазу сердечного сокращения и многое, многое другое.
Не каждый из перечисленных методов – обязателен, однако каждый из них имеет свои недостатки, даже такой, как УЗИ. Но у него может быть недостаток неожиданного характера. Это – гипердиагностика, или находка какого-то изменения в нормальном строении или функциях сердца, которые, кроме, как на экране аппарата, никак себя не проявляют: ребенок нормально растет и развивается, и совершенно не производит впечатления больного. Врач, который обратил внимание на такого рода отклонения, ни в коем случае не хочет вас запугать. Просто проверьте еще несколько раз, обоснованы ли возникшие опасения. Надо убедиться в том, что сейчас нет никакой непосредственной угрозы, и тогда – наблюдать и обследоваться чаще, чем это советуют детям, у которых ничего необычного в сердце нет.
Инвазивные методы: зондирование сердца и ангиокардиография
В отличие от неинвазивных, при этих методах необходимо ввести тонкую длинную трубочку-катетер в полости сердца ребенка, чтобы измерить давление в них «прямым» путем, а затем ввести в них контрастное вещество.
Не так давно зондирование и ангиокардиография были единственными, последними и решающими методами диагностики врожденных пороков. Сегодня это не так. Эхокардиография во многом уже вытеснила их, хотя и полностью не заменила. С другой стороны, инвазивные методы во многих ситуациях стали из чисто диагностических – лечебными, и позволяют иногда избежать значительно более травматичного хирургического вмешательства. О таких возможностях мы еще расскажем. А сейчас остановимся на некоторых важных моментах.
Зондирование будут происходить в специальном отдельном кабинете, где помещается рентгеноустановка. Вам туда заходить не разрешат, потому что условия процедуры предусматривают стерильность. В первый раз на всем протяжении обследования ребенок окажется без вас. Заранее, в палате, ему введут мягкое снотворное, чтобы он дремал. Сама процедура – катетеризация сердца – безболезненна, но введение катетеров требует пункции (т.е. прокола) сосудов, а иногда – и небольших разрезов.
Что же будут делать с ребенком? Через артерию и вену бедра ему введут в сердце катетеры, которые измерят давление в полостях сердца и возьмут пробы крови из камер, чтобы определить ее насыщение кислородом, а потом точно рассчитать величину сброса. После этого через установленные в сердце катетеры введут контрастное вещество и заснимут этот момент на пленку. Просмотр и анализ пленки позволит установить точный диагноз и составить план дальнейших действий. Процедура занимает около часа. Накануне вечером к вам, вероятно, подойдет специалист, который будет ее производить, и анестезиолог. В обязанность этих врачей входит объяснить вам, что будет сделано вашему ребенку, для чего и в какой последовательности. Они ответят на все ваши вопросы, поэтому не стесняйтесь их задавать. Поскольку не только этот момент, но и вообще любой визит с ребенком к врачам может быть для вас стрессом (а в стрессовой ситуации трудно оставаться собранным и разумным), то мы советуем заранее записывать не только ваши наблюдения и замечания, касающееся состояния ребенка, но и все возможные ваши вопросы: тогда вы не будете чувствовать себя растерянными, а после сожалеть о том, что от волнения забыли спросить или сказать что-то важное.
Результаты исследования будут обработаны, как правило, на следующий день и о них вам расскажет уже лечащий врач, который ведет ребенка.
Закономерности изменений показателей ультразвукового исследования при врожденных пороках сердца у плода в зависимости от особенностей внутрисердечной гемодинамики антенатального периода
ФГУ Научный центр акушерства, гинекологии и перинатологии им. В.И. Кулакова Минздравсоцразвития России,
Москва.

УЗИ сканер HS60
Профессиональные диагностические инструменты. Оценка эластичности тканей, расширенные возможности 3D/4D/5D сканирования, классификатор BI-RADS, опции для экспертных кардиологических исследований.
Врожденные пороки сердца редко влияют на развитие плода. Впервые это было отмечено в исследованиях B. Mac Mahon и соавт. [1]. Однако есть пороки, не совместимые с жизнью, и после рождения ребенок тотчас погибает. Некоторые врожденные пороки сердца, даже несложные формы, в раннем неонатальном периоде протекают злокачественно, обусловливая развитие декомпенсации кровообращения и дыхательную недостаточность. Главной причиной этого является несовершенство компенсаторных механизмов.
Диагностика врожденных пороков сердца у плода - одна из труднейших задач перинатологии. Многие врожденные пороки сердца, даже сложные, практически не совместимые с жизнью, антенатально не проявляются в силу особенностей внутрисердечной гемодинамики и после рождения становятся катастрофой для жизни ребенка.
Антенатальный период характеризуется особенностями кровообращения, такими как высокое давление в правом желудочке, незначительный объем кровотока в легочной артерии, параллельность работы желудочков сердца, функционирующие артериальный проток и овальное окно, нагнетающие кровь как обходные анастомозы в большой круг кровообращения за счет усиленной работы правого желудочка. Эти особенности внутрисердечной гемодинамики плода, безусловно, должны корректировать характер гемодинамических изменений ультразвуковых показателей сердца в норме и при пороках сердца у плода.
Известно, что у пациентов с врожденными пороками сердца нарушения гемодинамики в результате анатомических изменений в значительной степени влияют на данные ультразвукового сканирования сердца, такие как размеры полостей сердца, степень гипертрофии миокарда, функция клапанного аппарата, сократительная способность миокарда, направленность движения межжелудочковой перегородки.
Метод оценки внутрисердечной гемодинамики базируется на широко известных понятиях о систолической, объемной и смешанной перегрузках сердца, предложенных в 1952 г. E. Cabrera и J. Monroy [2].
В основе разделения использован следующий принцип.
Нагрузка сопротивлением возникает при ситуации, когда выброс крови из желудочков сердца в магистральные сосуды затруднен на уровне полулунных клапанов (стеноз аорты и легочной артерии), подклапанного пространства (идиопатический гипертрофический субаортальный стеноз, подклапанный стеноз аорты или легочной артерии), на протяжении сосудистого русла (коарктация аорты) либо при значительном увеличении выходного сопротивления (синдром Эйзенменгера). В результате затруднения выброса крови резко возрастает напряжение миокарда соответствующего желудочка при относительно стабильном объеме крови, что служит проявлением систолической перегрузки сердца. При систолической перегрузке желудочков сердца независимо от нозологической формы порока полость желудочка, несущего основную нагрузку сопротивлением, умеренно увеличивается в размерах. В ответ на нагрузку сопротивлением на эхокардиограмме выявляется гипертрофия миокарда соответствующего желудочка, и чем больше сопротивление выбросу, тем резче выражена степень гипертрофии миокарда соответствующего желудочка и межжелудочковой перегородки (рис. 1) [3].

Рис. 1. Систолическая перегрузка правого желудочка. Поперечное сечение желудочков сердца при стенозе легочной артерии. Градиент давления правый желудочек - легочная артерия равен 200 мм рт.ст. Выраженная гипертрофия межжелудочковой перегородки и миокарда передней стенки правого желудочка.
Нагрузка объемом возникает при дополнительном притоке крови в желудочки и в результате шунтирования крови через септальные перегородки или артериальный проток (дефекты межпредсердной и межжелудочковой перегородок, открытый артериальный проток), а также в результате обратного тока крови через атриовентрикулярные клапаны (клапанная недостаточность).
Характерными особенностями выраженной объемной перегрузки правого желудочка являются дилатация желудочка, при которой толщина миокарда не превышает верхней границы нормы, увеличение правого предсердия, парадоксальный характер движения межжелудочковой перегородки и увеличение амплитуды движения трикуспидального клапана (рис. 2, 3).

Рис. 2. Длинная ось сердца. Объемная перегрузка правого желудочка при дефекте межпредсердной перегородки. Объем сброса крови превышает 200% МОС. Отмечается выраженная дилатация правого желудочка.

Рис. 3. Объемная перегрузка правого желудочка при дефекте межпредсердной перегородки. В- и М-сканирование. Стрелкой показан парадоксальный характер движения межжелудочковой перегородки.
Для левого желудочка признаком объемной перегрузки являются увеличение полости левого предсердия и желудочка, а также экскурсии межжелудочковой перегородки и миокарда задней стенки левого желудочка (рис. 4).

Рис. 4. Объемная перегрузка левых отделов сердца. В- и М-сканирование. Отмечается усиление экскурсии межжелудочковой перегородки и миокарда задней стенки левого желудочка.
IVS - межжелудочковая перегородка, MLV - миокард левого желудочка, LV и RV - левый и правый желудочек.
При сочетании нагрузки сопротивлением и объемом возникает смешанная перегрузка (например, при дефекте межжелудочковой перегородки и повышении давления в легочной артерии для правого желудочка систолическая перегрузка сочетается с нагрузкой объемом, для левого желудочка в результате артериальновенозного сброса крови через дефект).
За многолетний период (с 1980 г. по настоящее время) наблюдений в ФГУ Научный центр акушерства, гинекологии и перинатологии им. В.И. Кулакова Минздравсоцразвития России было замечено, что в антенатальном периоде не всегда работают принципы гемодинамических эхокардиографических проявлений врожденного порока сердца, которые ранее были разработаны и представлены в современной литературе 6.
Анализ более 2000 наблюдений врожденных пороков сердца у плода показал, что в ряде наблюдений имеются лишь анатомические изменения, характерные для определенной нозологической формы порока. При других врожденных пороках сердца изменения на эхокардиограмме связаны с характером гемодинамической нагрузки на сердце и аналогичны тому, что наблюдается после рождения. Наконец, в ряде наблюдений врожденных пороков сердца у плода вторичные изменения на эхокардиограмме, вызванные гемодинамическими нарушениями, отличаются от гемодинамических проявлений ультразвуковых показателей у детей и взрослых. Это позволило разделить все врожденные пороки сердца плода на три группы в зависимости от изменений на эхокардиограмме, обусловленных особенностями антенатальной внутрисердечной гемодинамики.
В первую группу вошли пороки сердца, которые, имея отчетливые анатомические проявления патологии, при ультразвуковом исследовании не имеют гемодинамических проявлений врожденного порока сердца. К ним относятся: дефект межпредсердной перегородки, дефект межжелудочковой перегородки, общий желудочек, простая форма транспозиции магистральных сосудов и также при наличии дефекта межжелудочковой перегородки общий артериальный ствол, двойное отхождение сосудов от желудочков сердца.
- дилатации правого желудочка (см. рис. 2, 3);
- увеличению правого предсердия;
- парадоксальному характеру движения межжелудочковой перегородки (см. рис. 2, 3).
Антенатально при равных величинах давления в желудочках сердца и в предсердиях объемной перегрузки не возникает. В связи с этим ни один из эхокардиографических гемодинамических признаков, используемых у детей и взрослых, не выявляется у плода. К эхокардиографическим проявлениям порока антенатально относится только прямой признак - перерыв ультразвукового луча в области дефекта. Размеры сердца, соотношение размеров желудочков сердца не отличаются от нормы (рис. 5).

Рис. 5. Четырехкамерное сечение сердца плода. Стрелкой указан первичный дефект межпредсердной перегородки (АVS).
В равной степени это относится к дефекту межжелудочковой перегородки (рис. 6), простой форме транспозиции магистральных сосудов (рис. 7, 8), транспозиции магистральных сосудов с дефектом межжелудочковой перегородки (синдром Тауссиг - Бинга) (рис. 9), общему желудочку (рис. 10), общему артериальному стволу (рис. 10), двойному отхождению сосудов от одного из желудочков сердца (рис. 11).
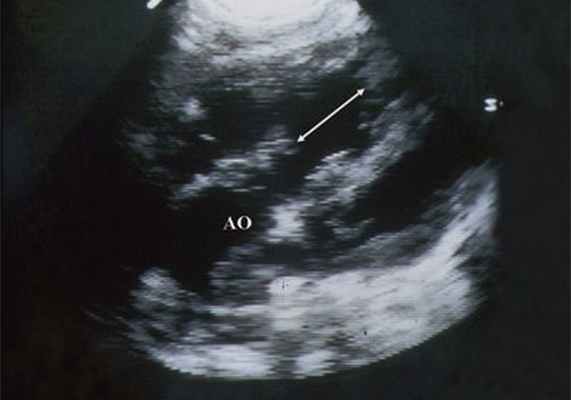
Рис. 6. Дефект межжелудочковой перегородки. Длинная ось сердца. Стрелками показан дефект межжелудочковой перегородки.

Рис. 7. Транспозиция магистральных сосудов.

Рис. 8. Транспозиция магистральных сосудов, стрелками показаны ветви легочной артерии.
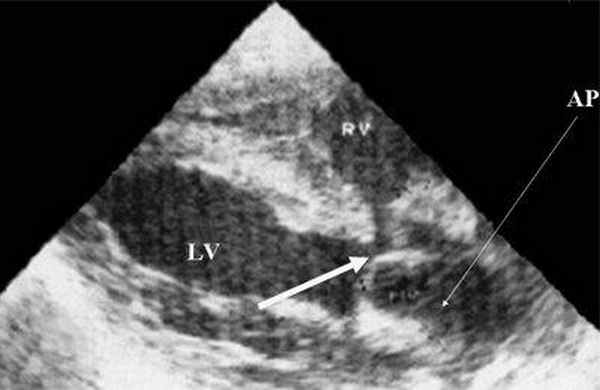
Рис. 9. Синдром Тауссиг - Бинга. Легочная артерия (отмечена стрелкой) расположена над дефектом межжелудочковой перегородки.
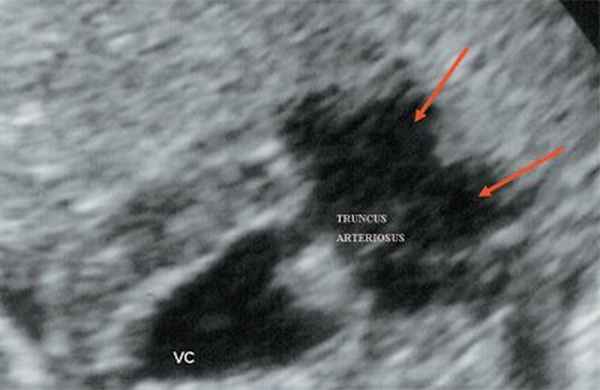
Рис. 10. Общий желудочек с отхождением TRUNCUS ARTERIOSUS. Стрелками показано разделение TRUNCUS ARTERIOSUS на аорту и ствол легочной артерии.
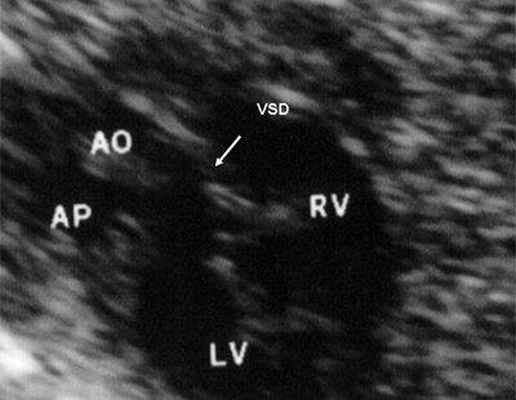
Рис. 11. Двойное отхождение магистральных сосудов от левого желудочка. Длинная ось сердца. Магистральные сосуды инвертированы и отходят от левого желудочка. Аорта расположена "верхом" над дефектом межжелудочковой перегородки (стрелка).
LV и RV - левый и правый желудочек, АР - легочная артерия, АО - аорта, VSD - дефект межжелудочковой перегородки.
Таким образом, диагностика перечисленных выше врожденных пороков сердца основывается на знании анатомических изменений, характерных для определенной нозологической формы патологии.
Вторая группа врожденных пороков сердца. При ультразвуковом исследовании регистрируются анатомические и гемодинамические изменения, характерные для определенной нозологической формы порока. В эту группу были отнесены: стеноз аорты, стеноз легочной артерии, врожденный митральный стеноз, транспозиция магистральных сосудов с сужением легочной артерии, обструкция опухолью выходного тракта одного из желудочков, аномалия Эбштейна, синдром гипоплазии правого и левого желудочков сердца, фиброэластоз, преждевременное закрытие овального окна.
Как пример можно разобрать изменения эхокардиографических показателей при клапанном стенозе легочной артерии. Нарушение гемодинамики при изолированном стенозе легочной артерии обусловлено препятствием на пути выброса крови в легочную артерию. Тяжесть стеноза определяется разницей систолического давления в правом желудочке и легочной артерии, т.е. градиентом давления.
При двухмерной эхокардиографии выявляется утолщение створок клапана легочной артерии, экскурсия их уменьшена, а в систолу они образуют купол. Это анатомические проявления порока. К ним добавляются гемодинамические проявления: выраженная гипертрофия миокарда передней стенки правого желудочка и межжелудочковой перегородки, значительно превышающие нормативы. Степень выраженности гипертрофии миокарда правого желудочка зависит от степени стенозирования легочной артерии и соответственно от величины градиента давления. Эти данные получены при сопоставлении результатов ультразвукового сканирования и данных катетеризации полостей сердца у детей [6]. Следует особо отметить, что при выраженной гипертрофии миокарда полость правого желудочка увеличивается незначительно. Отмечается также увеличение размера правого предсердия.
У плода получены аналогичные изменения, зависящие также от степени стенозирования легочной артерии. Полость правого желудочка, как видно на рис. 12, не увеличена. В то же время имеется значительная гипертрофия стенок правого желудочка. Как и в постнатальном периоде отмечено увеличение полости правого предсердия (рис. 13). После рождения при катетеризации полостей сердца в данном наблюдении был выявлен градиент давления на выходе из правого желудочка, равный 200 мм рт.ст.

Рис. 12. Стеноз легочной артерии. Гипертрофия миокарда правого желудочка.
Читайте также:
