Тромбоэмболические расстройства при беременности
Обновлено: 18.04.2024
В США тромбоэмболические состояния – тромбоз глубоких вен Тромбоз глубоких вен (ТГВ) Тромбоз глубоких вен (ТГВ) – это процесс свертывания крови в глубокой вене конечности (обычно это область голени или бедра) или таза. ТГВ является первичной причиной тромбоэмболии легочной артерии. Прочитайте дополнительные сведения (ТЭЛА) – ведущие причины материнской смертности.
Во время беременности риск увеличивается, поскольку
Емкость венозного русла и венозное давление в нижних конечностях увеличены, что приводит к застою.
Беременность вызывает определенную степень гиперкоагуляции.
Симптомы тромбофлебита или их отсутствие не являются патогномничными и не позволяют прогнозировать тяжесть заболевания или риск эмболии. Тромбоэмболические осложнения могут развиться бессимптомно, с минимальными симптомами или со значительными симптомами. Также отек икроножных мышц, их спазмы и болезненность, обычно возникающие во время беременности, могут имитировать признак Гоманса.
Диагностика
Допплеровская ультрасонография или КТ для диагностики ТГВ
СКТ для диагностики ТЭЛА
Диагноз ТГВ, как правило, устанавливают с помощью допплеровской ультрасонографии. В послеродовом периоде при отсутствии патологии по данным допплеровской ультрасонографии и плетизмографии, но подозрении на тромбоз подвздошных, яичниковых или других тазовых вен следует провести КТ с контрастированием.
Для диагностики ТЭЛА чаще используют СКТ, чем вентиляционно-перфузионное сканирование, потому что при КТ радиационная нагрузка ниже, а чувствительность одинакова. Если диагноз ТЭЛА сомнителен, следует выполнить ангио-графию легочной артерии.
Лечение
Такое же, как и вне беременности, но исключает варфарин
Для женщин с повышенным риском профилактически назначают низкомолекулярный гепарин на протяжении всей беременности и в течение 6 недель после родов
Если ТГВ или ТЭЛА выявлены во время беременности, антикоагулянтом выбора является низкомолекулярный гепарин (НМГ). НМГ, по причине молекулярного размера, не проходит через плаценту. Он не вызывает остеопороза и тромбоцитопении у матери, которая может развиться из-за длительного ( ≥ 6 месяцев) применения нефракционированного гепарина. Варфарин проникает через плаценту и может вызвать нарушения или гибель плода (см. таблицу Некоторые лекарства, оказывающие побочные эффекты при беременности [Some Drugs With Adverse Effects During Pregnancy] Некоторые лекарства, оказывающие побочные эффекти при беременности ).
Показания к тромболитической терапии при беременности те же, что и вне ее.
Если ТЭЛА развивается, несмотря на адекватную антикоагулянтную терапию, показано вмешательство обычно в виде установки кава-фильтра в нижней полой вене дистальнее почечных сосудов.
Если у женщин во время предыдущей беременности развивались ТГВ или ТЭЛА, или если присутствуют сопутствующие тромбофилические заболевания, им в целях профилактики назначают препараты НМГ (например, эноксапарин 40 мг подкожно 1 раз в день) с началом курса, когда беременность была впервые диагностирована, и продолжением до 6 недель после родов.
Основные положения
Во время беременности повышается риск тромбоэмболических нарушений, хотя большинство случаев тромбоэмболии развивается в послеродовом периоде вследствие травм сосудов при родоразрешении.
Симптомы тромбофлебита или их отсутствие не являются патогномничными и не позволяют прогнозировать тяжесть заболевания или риск эмболии.
Диагноз тромбоз глубоких вен устанавливают с помощью допплеровской ультрасонографии, однако после родоразрешения при отсутствии патологии по данным допплеровской ультрасонографии и плетизмографии, но подозрении на тромбоз тазовых вен, следует провести КТ с контрастированием.
Диагноз эмболии легочной артерии устанавливают с помощью спиральной КТ или, при необходимости, ангиопульмонографии.
Терапией выбора является низкомолекулярный гепарин (НМГ); варфарин следует избегать.
Женщинам с высоким риском необходимо назначить НМГ с профилактической целью сразу после установления факта беременности и продолжать на протяжении 6 недель после родов.
Авторское право © 2022 Merck & Co., Inc., Rahway, NJ, США и ее аффилированные лица. Все права сохранены.
Статьи
половины беременности, внутриутробной задержки развития плода, отслойки плаценты или инфаркта плаценты, ей показано проведение обследования на тромбофилию.
Гипергомоцистеинемия, которая развивается иногда под влиянием наследственного генетического полиморфизма, ассоциирована с поздним токсикозом и принимает участие в развитии инфарктов и отслойки плаценты. Воспаление эндотелиальной выстилки сосудов на фоне повышенного уровня гомоцистеина, вызывает повышенный риск как венозного, так и артериального тромбоза. К гипергомоцистеинемии может приводить наличие в организме измененных форм фермента метилентетрагидрофолатредуктазы (MTHFR), который в норме участвует в превращении гомоцистеина в метионин.
Наследственный полиморфизм фактора Лейдена (V), имеющий сильную предрасположенность к тромбозам, встречается с повышенной частотой у женщин с привычным невынашиванием.
Среди пациенток с привычным невынашиванием беременности, аномальные формы фактора V Лейден наиболее часто встречаются у женщин, имеющих выкидыши во втором триместре беременности.
Гипергомоцистеинемия сама по себе не имеет значительной ассоциации с потерей плода на раннем сроке беременности, что свидетельствует о том, что дефицит фолиевой кислоты и полиморфизм MTHFR могут действовать через дополнительные, пока еще неизвестные факторы. Повышенный уровень гомоцистеина также выявляется при беременностях, осложненных гестозом, и это повышение сохраняется после родов.
Другие причины плацентарного тромбоза.
Беременность может способствовать проявлению генетического дефекта, так как при ней развиваются следующие особенности:
- Физиологическое повышение коагуляции крови.
- Подавление растворения фибринового сгустка (фибринолиза).
- Снижение содержания и активности естественных антикоагулянтов крови.
- Повышение функциональной активности тромбоцитов.
- Эти изменения при беременности имеют охранительное значение, они предотвращают обильную кровопотерю в родах, но при этом они же провоцирую развитие тромбоза в сосудах плаценты, особенно при наличии врожденной патологии в системе гемостаза.
- Низкое сосудистое сопротивление плаценты и медленный кровоток в ее сосудах, является ключевым моментов в обеспечении хорошего кровоснабжения плода, но при этом создаются условия для отложения фибрина и образования тромбов.
- Нормальное увеличение уровня фибриногена и свертывающих белков во время беременности также может провоцировать тромбообразование. Понижение доступности фолиевой кислоты, поступающей с пищей, происходит при курении, и это может вызвать еще большее повышение уровня гомоцистеина.
Риск тромбоза при наследуемых формах тромбофилий может быть снижен путем применения небольших доз аспирина, гепарина, фолиевой кислоты, внутривенного введения иммуноглобулина G, или концентратов гематогенных факторов. Для носителей наследуемой тромбофилии с повторяющимися неблагоприятными исходами беременности, заслуживают внимания два варианта профилактического лечения: назначение низкомолекулярного гепарина (эноксапарина) женщинам с привычной поздней потерей плода и лечение фолиевой кислотой при тяжелом токсикозе 2-ой половины беременности.
У всех лиц - беременных и нет, потребление фолиевой кислоты значительно снижает уровень гомоцистеина. Эффективность является высокой в случаях, когда перед лечением уровень гомоцистеина был самым высоким и наименьшая, если уровень гомоцистеина был сравнительно небольшим. Уменьшение уровня гомоцистеина наблюдается при применении фолиевой кислоты в дозе от 0.5 мг до 5 мг в день в сочетании с витамином B6.
Высока вероятность тромбоэмболических осложнений и при наличии сердечнососудистых заболеваний, избыточной массы тела, анемии, перенесенном позднем токсикозе . Повышается риск тромбоза и у женщин в возрастной группе после 40 лет, при наличии злокачественных образований, малоподвижном образе жизни. Затяжные, длительные роды, кесарево сечение также предрасполагают к осложнениям. К группе очень высокого риска по развитию тромбозов, в том числе и в послеродовом периоде, относятся женщины с варикозной болезнью нижних конечностей.
Прежде всего, развитие послеродового тромбоза связано с изменениями в свертывающей системе крови. Во время естественных родов или кесарева сечения теряется кровь. Объем кровопотери может быть разным — от минимального (физиологического) до значительного (патологического), что зависит от конкретной ситуации. В любом случае, организм стремится прекратить дальнейшее истечение крови, вырабатывая большое количество факторов, способствующих повышению свертывания крови путем образования сгустков-пробок в просвете сосудов. И чем больше кровопотеря, тем активнее эти процессы. Кроме того, при отхождении плаценты или из-за механического повреждения тканей во время операции повреждается и стенка сосудов, происходит выбрасывание в кровь особых белков и ферментов эндотелия (внутренней выстилки сосуда), что также немаловажно для сдвига процессов в сторону повышения свертывания крови.
Для снижения риска венозных тромбоэмболических осложнений во время беременности рекомендуется применение низкомолекулярных гепаринов (НМГ) в профилактических и промежуточных дозах в виде подкожных инъекций. Однако в настоящее время решение о назначении НМГ беременным женщинам принимается лишь на основании наличия тромботического анамнеза или при выявлении той или иной тромбофилии (мутации фактор V Лейден, мутации протромбина, дефицита антитромбина, носительства антифосфолипидных антител и др.). Эти показания для назначения НМГ субъективны, поскольку они не основываются на точных лабораторных данных измерения избыточной (тромбоопасной) активации свертывания крови в разные сроки беременности. Соответственно, использование этих показаний приводит к неоправданно широкому применению гепаринов во время беременности.
Вероятность образования тромбов во время беременности увеличивают врожденная тромбофилия (состояние повышенной свертываемости крови), кесарево сечение, зрелый возраст роженицы и избыточный вес. Если женщина ранее рожала три и более раз или имеет многоплодную беременность (двойня и более) риск тромбоза также повышается. Дополнительными факторами риска образования тромбов выступают: гипертония, сердечно-сосудистые заболевания и сахарный диабет; применение оральных контрацептивов перед беременностью; обезвоживание.
Важно отметить, что риск образования тромбов сохраняется в течение двух месяцев после родов.
Лечение тромбозов - сложный процесс, который обязательно должен происходить под контролем врача. Поэтому при наличии факторов риска рекомендуется проводить профилактику тромбоза. Профилактика может быть немедикаментозная и медикаментозная. Врач определяет степень риска для каждого пациента – низкую, умеренную, высокую. После этого подбирается метод профилактики. Как правило, одной немедикаментозной профилактики людям с повышенным риском развития тромбоза мало, поэтому вместе с ней проводится медикаментозная профилактика. В этом случае применяются специальные препараты, препятствующие образованию тромбов.
Антифосфолипидный синдром (АФС) является причиной многих акушерских осложнений, таких как синдром потери плода, HELLP-синдром, преждевременные роды. Высокий риск неблагоприятных акушерских исходов при АФС обусловливает необходимость планирования беременности и подбора адекватной терапии беременной с данной патологией.
На сегодняшний день АФС является одной из актуальных проблем в акушерской практике. Клиническими проявлениями АФС в акушерстве являются синдром потери плода, задержка внутриутробного развития плода, HELLP-синдром, маловодие, фето-плацентарная недостаточность, преждевременные роды, гестоз (преэклампсия и эклампсия). Синдром потери плода на сегодняшний день рассматривается как специфический маркер АФС. Прерывание беременности при АФС может произойти на любом сроке беременности, и очень часто самопроизвольный выкидыш является единственным симптомом, позволяющим заподозрить АФС у пациентки.
Высокий риск неблагоприятных акушерских исходов при АФС диктует необходимость планирования беременности у данных пациенток, тщательного подбора медикаментозной терапии и постоянного контроля за состоянием матери и плода.
На этапе планирования беременности у пациентки с АФС необходимо исключить сопутствующие факторы риска развития тромбозов. Спектр профилактических мероприятий включает в себя коррекцию избыточного веса, лечение сопутствующей артериальной гипертензии, коррекцию нарушений липидного спектра, отказ от курения, а также использование компрессионного трикотажа при посттромбофлебитическом синдроме.
Беременным с АФС с момента зачатия назначают низкие дозы АСК (50-100 мг в сутки, но не более 150 мг в сутки ) и низкомолекулярные гепарины до момента родов. Отменяют низкомолекулярные гепарины за 12-24 часа до родоразрешения. Лечение гепаринами возобновляют через 12 часов после родов на срок не менее 4-6 недель.
Своевременная диагностика и адекватная терапия АФС у беременных, тщательный контроль за показателями системы гемостаза, регулярный контроль за состоянием плода, совместное ведение беременности акушером-гинекологом и смежными специалистами позволяет улучшить перинатальные исходы.
Основные принципы профилактики тромбоэмболических нарушений при беременности и в послеродовом периоде
-->Венозная тромбоэмболия (ВТЭ) включает в себя тромбоз глубоких вен и тромбоз легочной артерии, представляет собой одно из наиболее распространенных серьезных осложнений беременности и в настоящее время является ведущей причиной материнской заболеваемости и смертности в развивающихся странах мира. В последние два десятилетия появились новые данные, свидетельствующие о связи между ВТЭ и врожденными и приобретенными тромбофилиями, что, в свою очередь, осложняет проведение адекватной и доказательно обоснованной тромбопрофилактики.
Несмотря на все современные стратегии и методы профилактики сохраняется достаточно высокий уровень заболеваемости ВТЭ. Частота тромбоэмболии легочной артерии (ТЭЛА) у беременных с нелеченым тромбозом глубоких вен составляет 13-24%, смертность – 12-15%. При нелеченом тромбозе септических тазовых вен частота ТЭЛА достигает 33%.
В свою очередь, при своевременно и правильно назначенной терапии можно добиться снижения риска ТЭЛА до 0,7-4,5% и снижения риска материнской смертности до 0,7%.
Учитывая все вышеизложенное, необходимо ответить на несколько основных вопросов.
Почему в период беременности и в послеродовом периоде повышается риск тромбоэмболических осложнений?
Беременность и послеродовой период ассоциируются с повышенным риском развития ВТЭ – от 0,61 до 1,72 на 1000 родов. По сравнению с небеременными женщинами одного и того же возраста вероятность развития ВТЭ в 4-5 раз выше при беременности и после родов. Несмотря на различные данные, полученные в исследованиях, является очевидной связь между частотой ВТЭ и антенатальным и постнатальным периодом. Также следует отметить, что в послеродовом периоде частота ВТЭ повышается в 5 раз по сравнению с дородовым периодом.
Повышение риска развития ВТЭ во время гестации связано с тем, что во время беременности отмечаются все три элемента триады Вирхова: стаз, сосудистая травма и гиперкоагуляция.
Факторы, влияющие на повышение риска развития тромбоэмболии во время беременности:
- нарушения целостности сосудов таза (кесарево сечение);
- приобретенный дефицит антитромбина (нефротический синдром, преэклампсия);
- дисбаланс гормонов (синдром гиперстимуляции яичников, многоплодная беременность);
- тромбофилия;
- семейный анамнез ТЭ;
- возраст >35 лет;
- родов больше 3;
- ожирение;
- иммобилизация;
- курение;
- варикозная болезнь (флебиты);
- воспалительные заболевания кишечника (ВЗК);
- любое состояние, требующее введения постоянного катетера;
- повышение факторов свертывания (фибриноген, VII, VIII, IX, X);
- снижение протеина S;
- нарушение фибринолиза (плацента выделяет ингибиторы фибринолиза);
- венозный стаз и компрессия нижней полой вены.
Повышение внутрибрюшного давления и сдавление vena cava увеличенной маткой приводит к снижению скорости кровотока и повышению венозного давления в венах нижних конечностей. Кроме того, повышение концентрации циркулирующего в крови прогестерона наряду с усилением местного синтеза простациклинов и оксида азота приводит к увеличению емкости глубоких вен.
Описанные выше изменения вызывают относительное усиление венозного застоя, который нарастает с увеличением срока беременности. Кроме того, прослеживается тенденция к более выраженному застою в левой нижней конечности. Следует помнить, что снижение венозного тонуса в совокупности с поражением эндотелия и активация прокоагуляционной системы эндотелия могут сохраняться еще в течение 6 недель после родов.
Поражение эндотелия может произойти во время кесаревого сечения или в результате оказания оперативных манипуляций во время родов, также может ассоциироваться с такими осложнениями, как преэклампсия, в этиологии которой ведущая роль принадлежит эндотелиальной дисфункции. Наконец, даже физиологически протекающая беременность связана с прокоагуляционными изменениями системы гомеостаза. Активность большинства протромботических факторов возрастает, концентрация некоторых антикоагуляционных факторов снижается и одновременно снижается фибринолитическая активность.
Все вышеперечисленные изменения приводят к тому, что частота ВТЭ у женщин репродуктивного возраста возрастает с 1 случая на 10 000 в год до 1 на 1000 среди беременных и женщин после родов.
Как оценить риск тромбоэмболических осложнений при беременности и в послеродовом периоде?

В августе 2014 г. в «Европейском кардиологическом журнале» (European Society of Cardiology) были опубликованы рекомендации по диагностике и ведению тромбоэмболии легочной артерии.
Кроме того, the Royal College of Obstetricians and Gynaecologists (RCOG), the American College of Obstetricians and Gynecologists (ACOG) опубликовали обновленные рекомендации по ВТЭ и беременности.
В 2011 г. D. Schoenbeck и соавт. разработали шкалу стратификации риска во время беременности.
Особое значение стратификация риска и выделение наиболее значимых факторов, влияющих на увеличение риска ВТЭ, приобретают при наблюдении и родоразрешении беременных женщин, которые относятся к группе высокого перинатального риска.
К основным факторам риска в клинике экстрагенитальной патологии относят:
- тромбоз глубоких вен (ТГВ) в анамнезе;
- возраст >35 лет;
- ожирение;
- онкопатологию в анамнезе;
- вновь выявленную онкопатологию;
- химиотерапию;
- варикозное расширение вен;
- катетеризацию центральной вены;
- комбинированные оральные контрацептивы;
- прием эритропоэтина;
- ВЗК;
- нефротический синдром;
- антифосфолипидный синдром;
- системную красную волчанку, аутоиммунный гепатит, ревматоидный артрит;
- миелопролиферативные заболевания;
- врожденную тромбофилию;
- травму.
Что касается беременных с кардиальной патологией, то в отдельную группу следует выделить женщин, имеющих крайне высокий риск тромбозов с наиболее драматическим развитием.
К ним относятся пациентки, у которых:
Каковы риски для матери и плода при проведении антикоагулянтной терапии во время беременности?
Принимая решение о проведении антикоагулянтной терапии во время беременности, необходимо помнить о балансе двух основных составляющих: риска для плода и эффективности/безопасности для матери. Поэтому начнем с антагонистов витамина К: метаболиты данных препаратов проникают через плаценту и могут оказывать тератогенный эффект, вызывать геморрагические осложнения у плода и неврологический дефицит в будущем. В связи с этим следует прекратить прием антагонистов витамина К до 6-й недели беременности и заменить его на более безопасные НМГ.
Наиболее эффективным и изученным в этом отношении является эноксапарин (Клексан). Он значительно уменьшает риск развития варфариновой эмбриопатии. Необходимо подчеркнуть, что беременные были исключены из участия в клинических исследованиях оценки влияния новых оральных антикоагулянтов (НОАК), дабигтрана, ривароксибана, апиксабана, эдоксабана, так как все эти препараты проникают через плаценту, и степень их отрицательного воздействия на плод неизвестна, равно как и другие репродуктивные риски. Опубликованы отдельные результаты работ по применению фондапаринукса во время беременности. Известно, что он проникает через плаценту в малых количествах, но большинство опубликованных работ включают данные о начале применения этого препарата во втором триместре, а иногда и позже.
Нефракционированный гепарин (НФГ), НМГ и данапароид (гепариноид) не проникают через плаценту и безопасны для плода. Несмотря на то, что НФГ давно используется для профилактики и лечения тромбоэмболических нарушений, НМГ имеют ряд преимуществ: лучший профиль безопасности, низкую частоту кровотечений, гепарин-индуцированной тромбоцитопении, гепарин-ассоциированного остеопороза.
Рекомендации
1. Врач любой специальности, консультирующий женщину репродуктивного возраста, которая получает длительную/пожизненную терапию антагонистами витамина К или новыми прямыми оральными антикоагулянтами, обязан предоставить ей информацию о возможных рисках для плода.
2. При профилактике и лечении женщин с ТГВ в перипартальный период предпочтение отдают НМГ. Исключение составляют женщины с тромбоцитопенией, индуцированной гепарином – ГИТ (при данной беременности или в анамнезе), а также с выраженными нарушениями функции почек (в этом случае предпочтительнее назначение НФГ).
3. Если женщина, получающая НОАК, планирует беременность, необходимо перевести ее на производные кумарина или НМГ до зачатия. В случае несвоевременности переход на другой препарат должен быть проведен сразу, как только беременность подтверждена.
4. Если у женщины имеет место тяжелая аллергическая реакция на НФГ или НМГ, а также ГИТ, необходимо назначить данапароид или фондапаринукс. Особое внимание должно быть уделено правильной дозировке этих препаратов перед родоразрешением.
5. Всегда следует учитывать баланс двух основных составляющих: риска для плода и эффективности/безопасности для матери, основываясь на оценке безопасности антикоагулянтов по классификации FDA (табл. 2).

Каковы риски при проведении антикоагулянтной терапии в период грудного вскармливания?
Ни метаболиты варфарина, широко применяющегося в США и Великобритании, ни метаболиты аценокумарола, более часто применяющегося в ЕС, не определяются в грудном молоке. То есть назначение ни одного из этих препаратов не приводит к антикоагулянтным эффектам у новорожденного, мать которого получает данные антикоагулянты в период лактации. Небольшие количества НМГ определялись в грудном молоке, однако необходимо помнить, что биодоступность гепарина при пероральном применении минимальна, поэтому вряд ли присутствие метаболитов НМГ в молоке будет иметь клинический эффект для новорожденного.
До сих пор нет убедительных данных об экскреции метаболитов фондапаринукса в грудное молоко кормящих женщин, поэтому возможные эффекты для новорожденного неизвестны.
Тем не менее производитель настаивает на крайне осторожном применении фондапаринукса при грудном вскармливании, что означает его отличие от воздействия пероральных форм гепаринов.
В литературе не представлено данных о влиянии НОАК на новорожденного при грудном вскармливании, однако производители настаивают на невозможности применения этих препаратов в период лактации.
Согласно руководству по профилактике тромбозов (в отличие от полных схем антикоагулянтной терапии), в 2008 г. рекомендациями ACCP были выделены профилактические и средние дозы гепарина. Средние дозы НФГ вводят подкожно каждые 12 ч с учетом показателей анти-Xa, которые должны соответствовать 0,1-0,3 ед/мл, или НМГ в дозе 40 мг, которые назначаются каждые 12 ч.
В последних рекомендациях RCOG и ACCP определены принципы идентификации дозирования НМГ как профилактической и средней дозы и схемы дозирования НФГ в тех случаях, когда НМГ не могут быть использованы или когда предпочтительнее НФГ (например, у пациентов с нарушением функции почек). Напротив, в последних рекомендациях RCOG выделен «низкодозированный» режим НФГ и «профилактический» режим НФГ и НМГ. Полные режимы антикоагуляции называются скорректированной дозой по ACCP и лечебной или терапевтической по RCOG и ACOG.
На сегодняшний день есть результаты исследований последовательных уровней анти-Ха. Пиковые уровни анти-Ха были ниже у беременных женщин по сравнению с небеременными, различие было связано с увеличением клиренса эноксапарина. Хотя пиковые уровни анти-Xa на стабильной дозе 40 мг эноксапарина снизились с 0,47±0,13 МЕ/мл в I триместре до 0,32±0,08 МЕ/мл в III триместре беременности (p=0,002), оба этих средних значения находились в пределах рекомендованного диапазона руководства по профилактике тромбозов. В настоящее время не существует минимального значения анти-Ха активности с доказанным эффектом предотвращения тромбоза. В одной из публикаций представлены данные 321 анти-Ха у 77 пациентов, получавших НМГ в качестве профилактики ВТЭ. В группе, где 62% пациенток получали НМГ 2 р/день, только 59% находились в диапазоне профилактики (определяемой как 0,2-0,4 МЕ/мл), несмотря на корректировки последовательных доз, а 26% были ниже и 15% – выше необходимого уровня. Очевидно, что правильным подходом в группе высокого риска (механические искусственные клапаны сердца) является титрование доз НМГ под контролем анти-Ха, что было предложено в 2016 г. на 4-м Конгрессе «Кардиальные проблемы при беременности».
Рекомендации
1. НФГ, НМГ, варфарин и аценокумарол могут применяться у кормящих женщин.
2. НОАК не должны быть использованы в период лактации.
Как правильно проводить антикоагулянтную терапию во время беременности и в послеродовом периоде?
Решения, касающиеся профилактического применения антикоагулянтов во время беременности и послеродовом периоде, напрямую зависят от баланса риска развития ВТЭ и риска профилактики тромбоэмболических осложнений.
Для обеспечения успеха медикаментозной тромбопрофилактики необходимо определить группу высокого риска развития ВТЭ, так как именно у этих пациентов в соотношении польза/риск всегда будет превалировать польза.
В современных шкалах тромбоэмболических осложнений (Caprini, Khorana A.) учитываются факторы, необходимые для более точного расчета вероятного риска. К ним относятся: наличие ВТЭ в анамнезе; наличие ВТЭ в семейном анамнезе; наличие диагностированной тромбофилии и ее клинических факторов; кесарево сечение; длительная дородовая иммобилизация; увеличение индекса массы тела, а также значительные осложнения беременности и сопутствующие заболевания.
Необходимо подчеркнуть, что тромбопрофилактика во время беременности, как правило, включает в себя подкожные инъекции НМГ в течение длительного времени, то есть имеет место «медикализация» беременности. Несмотря на то что профилактическая терапия НМГ является безопасной для плода и значительно снижает риск неблагоприятных исходов для матери, все-таки она остается достаточно затратной, требует инъекций, а порой и проведения планового родоразрешения, чтобы сделать возможной эпидуральную анестезию.
Особенно следует подчеркнуть, что во время беременности необходимая доза НМГ разделяется на два введения в сутки.
Нами предложен пошаговый подход к проведению тромбопрофилактики.
Шаг 1. Определить факторы риска ВТЭ.
Шаг 2. Определить метод тромбопрофилактики. Выявить наличие противопоказаний к проведению.
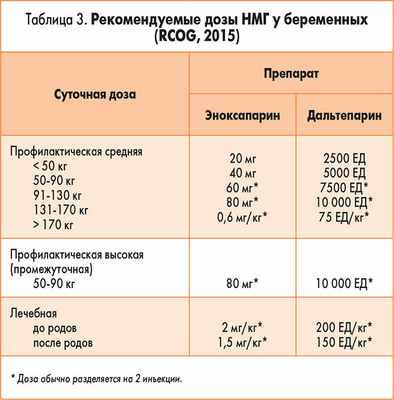
Шаг 3. Ввести необходимые препараты в адекватной дозе (табл. 3).
Шаг 4. Оценить эффективность, выявить необходимость дополнительных методов или препаратов.
Целесообразным является проведение аудита эффективности проведенной профилактики. Такой подход позволяет усовершенствовать и оптимизировать лечение, что, в свою очередь, приведет к уменьшению заболеваемости и смертности от ВТЭ.
Тематичний номер «Гінекологія, Акушерство, Репродуктологія» № 2 (22) червень 2016 р.
СТАТТІ ЗА ТЕМОЮ Акушерство/гінекологія
Представляємо вашій увазі рекомендації Німецького, Австрійського й Швейцарського товариств акушерства та гінекології щодо діагностики та лікування вульвовагінального кандидозу. У публікації проаналізовано й роз’яснено всі суперечливі твердження та надано рекомендації щодо ведення пацієнтів із гострим та хронічним рецидивуючим вульвовагінальним кандидозом. Ключові слова: вульвовагінальний кандидоз, Candida albicans, гострий вульвовагініт.
Запальні захворювання органів малого таза є однією з основних медичних проблем у гінекології, вирішення якої потребує вдало підібраної антибіотикотерапії. Тетрацикліни є одними з ранніх класів антибіотиків, які мають широку антимікробну активність та повну перехресну стійкість. Вони активні щодо практично всієї грампозитивної флори, грамнегативних коків (у т.ч. гонококів), кишкової палички, бактерій роду Enterobacter, клебсієли, а також дуже поширених останнім часом хламідій та мікоплазми. У статті представлені сучасні дані щодо використання цих препаратів у практиці лікаря-гінеколога. Ключові слова: тетрацикліни, доксициклін, гліцилцикліни, тайгециклін, запальні захворювання органів малого таза.
Незважаючи на наявність надійного тестового контролю, сучасні методи лікування та профілактики, рак шийки матки займає лідируючі позиції у структурі онкологічної патології. Ця тема не лишилася поза увагою під час Всеукраїнської науково-практичної конференції з міжнародною участю «Актуальні питання сучасного акушерства та гінекології», що відбулася минулого року. У рамках заходу асистент кафедри терапії та сімейної медицини Навчально-наукового інституту післядипломної освіти Тернопільського національного медичного університету ім. І. Я. Горбачевського, кандидат медичних наук Юлія Богданівна Якимчук спільно зі співавторами О. М. Якимчук та Т. В. Рудик висвітлили сучасні лікувальні стратегії при виявленні патологічного цитологічного мазка шийки матки. Ключові слова: рак шийки матки, кольпоскопія, вірус папіломи людини, цервікальна інтраепітеліальна неоплазія.
Вірус папіломи людини (ВПЛ) є основною причиною раку шийки матки вже понад 25 років. Повідомляється, що приблизно 5,5-11% усіх видів раку шийки матки є ВПЛ-негативними, що можна пояснити як відсутністю асоціації із ВПЛ-інфекцією, так і хибнонегативними результатами тестування. ВПЛ-негативний рак шийки матки часто діагностується на занедбаній стадії й має поганий прогноз, тому ведення цих випадків потребує більшої уваги. Ключові слова: вірус папіломи людини, рак шийки матки, ВПЛ-негативний рак шийки матки, аденокарцинома шийки матки.
ВЕНОЗНЫЕ ТРОМБОЭМБОЛИЧЕСКИЕ ОСЛОЖНЕНИЯ: КТО ВИНОВАТ И ЧТО ДЕЛАТЬ?
Венозные тромбоэмболические осложнения, к которым относятся: тромбоз глубоких вен, тромбоз подкожных вен, тромбофлебит и тромбоэмболия легочных артерий, на протяжении длительного времени являются важнейшей клинической проблемой.

По статистике, около 100 тысяч пациентов в РФ ежегодно погибают от внезапной тромбоэмболии легочной артерии. Тромбоэмболия представлена тромбами, образующимися в просвете сосудов и разносящимися с потоком крови по организму. Чаще всего тромбы образуются в просвете вен нижних конечностей, а затем попадают в правую половину сердца и далее в артерии лёгких.
В РФ ежегодно фиксируется около 80 000 новых случаев венозных тромбоэмболических осложнений. В течение месяца после тромбоза глубоких вен от легочной эмболии умирают 6% пациентов, но даже благополучный исход острого периода не означает исчезновения данной проблемы. После тромбоза в отдалённом периоде формируется посттромботическая болезнь, обусловленная органическим поражением глубоких вен и проявляющаяся нарушением венозного оттока крови. После тромбоэмболии легочных артерий развивается окклюзия или стеноз артерий - хроническая постэмболическая легочная гипертензия, чреватая развитием хронического легочного сердца. После массивной ТЭЛА в течение последующих 5 лет погибает 10-15% больных.

Механизм прижизненного образования тромбов внутри сосудов описывается триадой, открытой в 1856 году немецким морфологом Рудольфом Вирховым, которая включает в себя повреждение сосудистой стенки, замедление кровотока и повышение вязкости (свертывающей способности) крови.
Наиболее значимыми факторами для возникновения венозного тромбоза является гемодинамические нарушения (замедление кровотока) и гиперкоагуляция (повышенная свертываемость крови).
Вероятность венозного тромбоза увеличивается, в случае если у человека имеется врожденная или приобретенная тромбофилия, т.е. состояние, характеризующееся склонностью к тромбообразованию. С наличием тромбофилии могут быть связаны многие случаи “неожиданного” венозного тромбоза и легочной тромбоэмболии (в частности, возникающие у лиц молодого возраста, не имеющих серьезных клинических факторов риска). Инициировать тромбоз у пациентов с тромбофилией могут оперативные вмешательства, травмы, беременность и роды, т.е. те состояния, которые сопровождаются повреждением тканей, изменением тонуса сосудов, гормонального фона.
- - тромбофилии (наследственные или приобретенные);
- - эпизоды ВТЭО в анамнезе;
- - текущий онкопроцесс;
- - травмы и оперативные вмешательства;
- - увеличение возраста (старше 40 лет), чем старше человек, тем больше вероятность тромбообразования;
- - наследственность (наличие кровных родственников, имеющих в анамнезе тромбозы до 50 лет);
- - избыточная масса тела и ожирение;
- - варикозная болезнь нижних конечностей;
- - приём эстрогенсодержащих препаратов (оральная контрацепция, гормонозамещающая терапия в постменопаузальном периоде);
- - беременность и ближайший послеродовый период (6 недель) характеризующиеся значительными гормональными изменениями, преобладанием эстрогенов в крови, гемоконцентрацией, что приводит к значительному повышению свертывающей активности крови;
- - длительный постельный режим, иммобилизация (гипс, скелетное вытяжение) более 3 суток, длительное авиа или автопутешествие (более 8 часов) приводят к венозному застою вследствие отсутствия активности мышечно-венозной помпы голени;
- - острые воспалительные заболевания (пневмония, колит), сепсис;
- - сдавливание вен объёмным образованием (чаще всего на уровне малого таза), что приводит к значительному нарушению венозного кровотока и стазу крови;
- - хронические заболевания: сахарный диабет, артериальная гипертензия.

Тромбоэмболия легочной артерии имеет проявления различной степени выраженности. Иногда в силу незначительности симптоматики ТЭЛА мелких ветвей может остаться нераспознанной, приводя к осложнениям со стороны лёгких и сердца, например, к развитию хронической тромбоэмболической легочной гипертензии. Обычно ТЭЛА мелких ветвей сопровождается приступами сухого кашля или кровохарканья с болью в грудной клетке различной локализации. Часто у пациента отмечаются приступы внезапной одышки и чувство нехватки воздуха. Массивная ТЭЛА характеризуется выраженным болевым синдромом в грудной клетке, одышкой, кровохарканьем и цианозом (посинением) кожи лица, шеи, мочек ушей и груди строго до горизонтальной линии между сосками. Мгновенно может наступить клиническая смерть, без лечения переходящая в биологическую смерть.
Поставить правильный диагноз, установить причину тромбоэмболических осложнений, определить тактику ведения после случившегося тромбоза или назначить тромбопрофилактику при имеющихся факторах риска, оценить риск тромботических событий перед началом приёма гормональной терапии, планируемых оперативных вмешательствах, сможет только специалист.
В ГАУ РО ОКДЦ работают врачи-гематологи, терапевты-гемостазиологи, прошедшие специальную подготовку по патологии свертывающей системы крови, в распоряжении которых имеется современная высококачественная лабораторная диагностика. Врачи центра патологии гемостаза могут определить тактику ведения пациента; подобрать соответствующую терапию; снизить риск возможных осложнений; определить необходимость лабораторного контроля эффективности терапии.
Специалисты Центра патологии гемостаза в ГАУ РО ОКДЦ помогут Вам, своевременно распознать нарушения в системе гемостаза и при необходимости подберут эффективное лечение, подходящее в каждом конкретном случае.
Татьяна Николаевна Абрамова,
врач-терапевт- гемостазиолог высшей категории.
Беременность и риск тромбоза
Тромбоз глубоких вен — это образование сгустка (тромба) в просвете сосуда (в данном случае глубоких вен, расположенных в толще мышц нижних конечностей), который вызывает нарушение кровообращения. Болезнь проявляется распирающей болью, покраснением и отеком в месте тромбоза. Болезнь может протекать как бессимптомно, так и привести к жизнеугрожающему осложнению – тромбоэмболии легочной артерии 1 .

Женщины в меньшей степени подвержены риску развития венозного тромбоза, однако, во время беременности вероятность его возникновения значительно возрастает. Виной тому изменение гормонального фона, сдавление вен таза увеличенной маткой, нарушение баланса свертывающей системы крови, что может привести к патологическому тромбообразованию в венах 2 .

С первых дней беременности организм будущей мамы претерпевает серьезные изменения: происходит гормональная перестройка, могут снижаться показатели гемоглобина, ферритина, витамина В12, увеличиваются показатели холестерина, инсулина, щелочной фосфатазы, изменяется объем циркулирующей крови (таким образом организм адаптируется к развитию плода и последующим родам), перестраивается кровеносная система, а органы начинают работать «за двоих».

Тромботические осложнения – основная прямая причина материнской смертности во время беременности и в послеродовый период: 12,8% от всех смертей рожениц 3,6 . Поэтому необходимо пристально следить за здоровьем женщины во время беременности.
Основные факторы риска развития тромбоза у беременных
Врожденные аномалии сосудов и системы свертывания крови
Применение оральных контрацептивов и гормональная терапия
Cдавление вен малого таза
Хронические заболевания сердечно-сосудистой системы
Беременность и послеродовый период
Возраст более 35 лет
Малоподвижный образ жизни
Основные факторы риска развития тромбоза у беременных

Основные факторы риска развития тромбоза у беременных

Ключевые симптомы тромбоза 4
Почти всегда заболевание на ранних стадиях протекает без симптомов. Однако, можно выделить некоторые распространенные признаки тромбоза:


Как обезопасить себя?

Отказаться за 6 месяцев до планируемой беременности от оральных контрацептивов и других препаратов, влияющих на свертываемость крови для снижения риска тромбообразования.

Во время планирования и протекания беременности регулярно консультироваться с врачом, тщательно выполняя все его рекомендации, направленные на укрепление здоровья мамы и малыша 4 .
График посещения врача беременными 3,5


Подготовка к визиту 3
При планировании беременности помимо лечащего врача вы можете также проконсультироваться с врачом-гематологом или любым другим специалистом, который занимается проблемой тромбоза и гемостаза во время беременности. Стоит вспомнить, какие из анализов вы сдавали в последние пару месяцев: это поможет доктору отследить динамику вашего состояния.
Лабораторное исследование системы гемостаза
Для профилактики тромботических осложнений во время беременности в ряде случаев врачи некоторым беременным пациенткам могут порекомендовать пройти лабораторное исследование с оценкой свертывающей системы крови - Коагулограмма с показателями таких факторов свертываемости как 2-4 :
- Фибриноген — фактор свертывания крови, превращается в фибрин, последний впоследствии образует тромб.
- Количество тромбоцитов – клеток, непосредственно участвующих в процессе свертывания крови.
- Активированное частичное тромбопластиновое время (АЧТВ) - время, за которое формируется сгусток в крови, после добавления к ней специальных активаторов этого процесса.
- МНО (международное нормализованное отношение) — используется для комплексной оценки кровеносной системы пациента, показывает, насколько “жидкая” кровь.
Продемонстрируйте врачу список всех препаратов, которые вы регулярно принимали в течение последних двух месяцев. Эта информация очень важна!
Необходимо заранее изучить, болели ли ваши родственники какими-либо заболеваниями, связанными с повышенной свертываемостью крови и образованием тромбов в венозном русле, а также болезнями почек и сердечно-сосудистой системы.
Если вы ведете трекинг фитнес-активности, можно предоставить эти данные своему лечащему врачу.

Во время беременности при отсутствии противопоказаний при возможности стоит сохранять достаточно активный образ жизни. Небольшие физические нагрузки, такие как плавание и длительные пешие прогулки, только помогут вам и вашему будущему малышу быть здоровыми.

В качестве диеты рекомендуется употреблять в пищу продукты с низким содержанием холестерина, например: отруби, рыба, овощи, фрукты, в пище также должны присутствовать животные жиры.

Необходим тщательный сбор гинекологического анамнеза: истории предыдущих родов, процедур ЭКО или абортов.
Однако, эти данные почти всегда фиксируются в ваших амбулаторных картах и стоят отдельного уточнения только в случае, если ваши медицинские данные так или иначе были утеряны

Самое главное - регулярно посещайте врачей и медицинские центры, сдавайте все необходимые анализы, следуйте всем назначенным рекомендациям. Помните, что на ранних этапах можно предотвратить серьезные осложнения.

Во что бы то ни стало стоит отказаться от всех вредных привычек.
Получить консультацию профильного специалиста
И пройти специализированное обследование системы гемостаза можно в медицинских центрах, представленных на карте
Источники
- Furie B, Furie BC (2008). «Mechanisms of thrombus formation». New England Journal of Medicine 359 (9): 938–949. DOI:10.1056/NEJMra0801082. PMID 18753650.
- A comparative study of blood fibrinolytic activity in normal women, pregnant women and women on oral contraceptives. J Obstet Gynecol Br Commonw, 77 (1970), pp. 752-756
- Акушерство. Национальное руководство. Под ред. Э.К. Айламазяна, В.И. Кулакова, В.Е. Радзинского, Г.М. Савельевой 2009г.
- Kahn SR, Lim W, Dunn AS, Cushman M, Dentali F, Akl EA et al; American College of Chest Physicians. Prevention of VTE in nonsurgical patients: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest 2012; 141(2 Suppl): e195S-226S. [PMC free article] [PubMed]
- Weiss J., Smith R. S. // Акушерство и гинекология: диагностика и лечение: Пер. с англ.; Под ред. А. Н. Стрижакова.— М., 2008. — Т. 1. — С. 729—759.
- MBRRACE-UK. Mothers and Babies: Reducing Risk through Audits and Confidential Enquiries across the UK Saving Lives, Improving Mothers’ Care - Surveillance of maternal deaths in the UK 2011-13
Сайт предназначен только для посетителей из Российской Федерации
Дата последнего обновления: 17.01.2020 «ВСЕ ПРАВА ЗАЩИЩЕНЫ»
*Под диагностикой и лечением понимаются исключительно диагностика и лечение специалистом. Пожалуйста, проконсультируйтесь с Вашим лечащим врачом
Сайт предназначен только для посетителей из Российской Федерации Дата последнего обновления: 21.01.2020
*Под диагностикой и лечением понимаются исключительно диагностика и лечение специалистом. Пожалуйста, проконсультируйтесь с Вашим лечащим врачом
ПЕРЕХОД НА ВНЕШНИЙ РЕСУРС
Вы покидаете сайт Представительства АО «Санофи-авентис груп» (Франция) и переходите по ссылке, предоставляемой в информационных целях. Представительство АО «Санофи-авентис груп» (Франция) не несет ответственности за информацию, размещенную на внешних ресурсах и не осуществляет проверку размещенной на них информации.
Читайте также:
- Сочетанные эндоскопические исследования. Сочетанное лапароколоноскопическое исследование
- Ишемическая оптическая нейропатия
- Почему мерзнут ноги и руки даже в тепле? От чего ладони и ступни постоянно холодные?
- Опухоль фолликулярной воронки. Трихоэпителиома.
- Синдром ретроградной артериальной перфузии. Акардия у одного из близнецов
